無菌医薬品について
無菌医薬品には注射により投与する注射剤、透析により投与する透析剤、目に投与する点眼剤などがあります。製剤に直接接する直接容器は、製剤の品質を維持したり、使用者の利便性を確保する機能を有し、アンプル、バイアル、カートリッジ、輸液バッグ、プレフィルドシリンジ(PFS)、ブローフィルシール(BFS)、フォーム・フィル・シール(FFS)、プラスチック容器などがあります。無菌性確保のため無菌医薬品は最終滅菌法または無菌操作法で製造されます。バイアルやシリンジなど種々の容器を扱う場合は、あらかじめ洗浄滅菌された直接容器が専用ケースにセットされたネストと呼ばれる直接容器の供給形態が使用されることもあります。この場合充填機などの装置もネスト専用となりますが容器の切替えが容易なのが特徴です。充填された中間製品は単一、または複数のフィルム・紙などで包装され法令に規定された表示(ロット番号、使用期限、バーコードGS1など)を施され、輸送時を含めて製剤の品質を維持するとともに、使用時の過誤防止並びに利便性が確保されています。
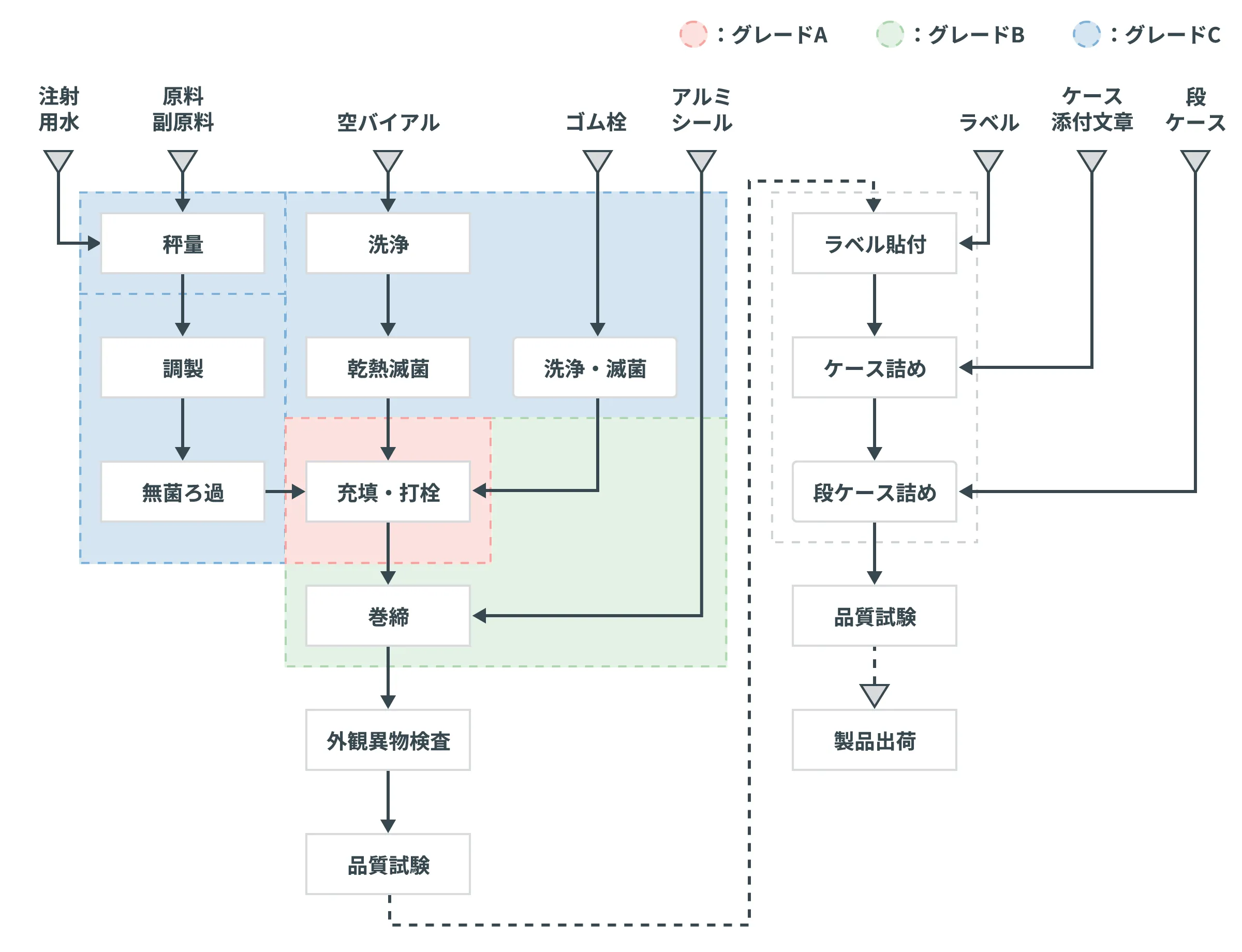
無菌医薬品の製造工程の一例
図に無菌医薬品の一例としてバイアル液注品の無菌操作法による工程フロー図を示します。
工程フロー図の例:
バイアル液注品の無菌操作法での製造工程の例
- 原料の秤量、調製、直接容器の洗浄から充填・打栓・巻締までは微生物汚染、異物混入防止等のため、適切な微粒子数、温度湿度に制御されたクリーンルームで行われます。特に充填・打栓工程は重要区域としてグレードAの清浄度環境下で行われます。
- バイアルは乾熱滅菌トンネルで脱エンドトキシン(パオロジェン)処理がされ、ゴム栓は専用装置で洗浄、滅菌が行われ、調製液は無菌ろ過フィルターを介して充てん装置に供給されます。
- 巻締めされた中間製品は、外観異物検査機により全数が外観および内用液中の異物が検査され、抜き取りされたサンプルの無菌試験を含めた品質試験が行われます。
- 品質試験に適合した中間製品は包装工程でロット番号、使用期限等が印字されたラベルが貼付され、必要な情報が印刷されたケースに詰められ、ロット番号、使用期限等が印字がされます。最終試験に適合したロットが出荷されます。
無菌医薬品製造設備の
キーポイント
製造工程と清浄度クラス・グレード管理の考え方
充填は従来より無菌室内に作られたグレードA環境で行われてきましたが、新規設備を導入する場合、汚染源の最大のリスクの一つである作業者との接触を完全に遮断するアイソレータや無菌接続ポート(RTP)の技術をグレードC/D環境に導入するケースが増えてきています。グローブリークテスター、除染装置、微粒子モニタリング装置など周辺装置が必要です。除染のためには、空調システムとの調整が必要となります。
作業者の安全
病原性の高いバイオ医薬品などの増加で、製品品質に加え作業者安全の観点から調製や充填設備の排気にもHEPAフィルターを備えたアイソレータを使用したコンテイメント性能が要求されてきています。稼働時、除染時のアイソレータ内外、充填室内外の差圧、気流の設計が必要となります。また、充填後のバイアルの外面を洗浄する外洗装置を必要に応じて導入することになります。
リークテスト/完全性の保証

容器の完全性につきましてはバイアルの場合はゴム栓部からのリークを防ぐ目的で空バイアルの口部をカメラで検査し、ゴム栓打栓装置、巻締装置の各種パラメータを全数モニターして完全性を保証します。リスクに応じて自動検査する容器リークテスターも数社から選択することもできます。アンプルなどの溶融して閉栓する容器の場合は、乾式または湿式のピンホール検査機で全数を検査します。
異物混入のリスク対応

異物の混入は重大な品質リスクですので、容器が閉栓されるまでは各装置で異物混入防止策を講じます。また、洗浄機の洗浄機能の監視も必要となります。充填供給部でガラス容器が破損した場合は検知装置と周辺容器をグローブ越しに回収することができるように設計することが重要です。充填後に外観異物検査機を導入する場合は液中の気泡や製剤の内容物から外来性異物を判別検査できることを事前にメーカーに確認することが必要です。検査機では良品誤検知を極力減らし、排除された異物を確認し、データ化することが異物低減に繋がります。
無菌接続の装置
ゴム栓の洗浄滅菌装置ではRTPを備えたベッセルでゴム栓の洗浄、滅菌、乾燥を行い、充填打栓装置のアイソレータに専用のリフターを使用して無菌接続できる装置が各社からラインアップされています。ベッセルの大きさと滅菌回数、アルミキャップも滅菌対象とするか、リフターの設置方法、設置スペースなどを検討する必要があります。
医療事故防止、トレーサビリティ
包装では医薬品の取り違えによる医療事故の防止及びトレーサビリティの確保のためバーコード表示が義務化され、包装工程での印字・検査装置が必要となっています。また、海外へ輸出する場合は、対象国の規制に沿った表示の対応が必要となります。
偽薬防止技術

単価の高い医薬品で、海外へ輸出される製品などは表示材料などへ偽薬防止技術が施されることがあります。
コンタミネーション防止対策

異種品コンタミ防止のため、生産スペースの区画とレイアウト及び生産開始・終了時にラインクリアランスがやり易い設備仕様とします。検査装置が増えることに伴い、系列外排除品が増えることになりますが、不良品の混入のリスクを排除させるためには極力誤検知品を少なくすることと、排除品を処理する十分なスペースを計画することが重要です。また、容器の洗い直しを行う共有の洗い場や、容器を運ぶ製品缶内の残存確認への配慮が必要です。
シーエムプラスのつよみ
①エンジニアリング+CM方式
CM方式は、プロジェクトを成功に導くために、QCD(品質、コスト、工程)+EHS(環境、衛生、安全)の各々の観点で、発注者お客様、設計者と一体となって透明性を持って、プロジェクトを運営管理する方式です。マネジメントを専門に行うCMr(コンストラクション・マネジャー)を始めとするプロフェッショナルが、お客様の立場で業務を行います。
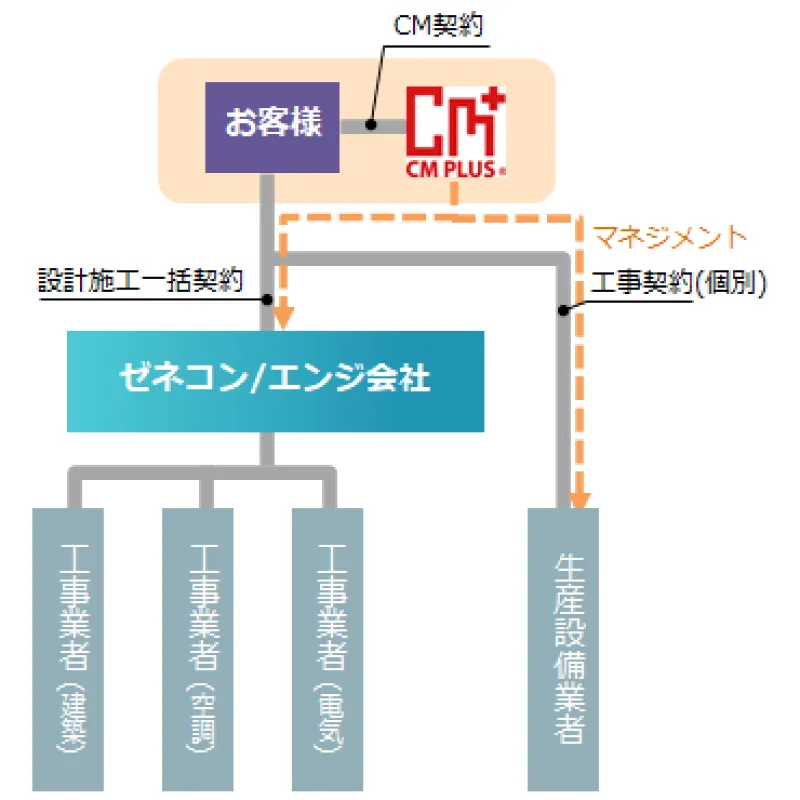
CM Plusでは、エンジニアリング(設計)を社内で行います。製造プロセス、機器・設備、建築並びに製造支援設備(電気・空調・ユーティリティ等)に精通したエンジニアを擁しており、計画初期段階から施設全体を俯瞰しますので、統合性のあるレイアウト施設の構築が可能です。
②生産機器と建築設備のトータルでの調整
生産機器のライン構築、レイアウトや内部動線/物流といった内面から建築設備を展開していくなど、生産プロセス中心の視点で設計を遂行していくため、生産システムと調和の採れた原薬工場を設計、建設します。又、生産システムのソフト面まで踏み込んだ計画を行います。
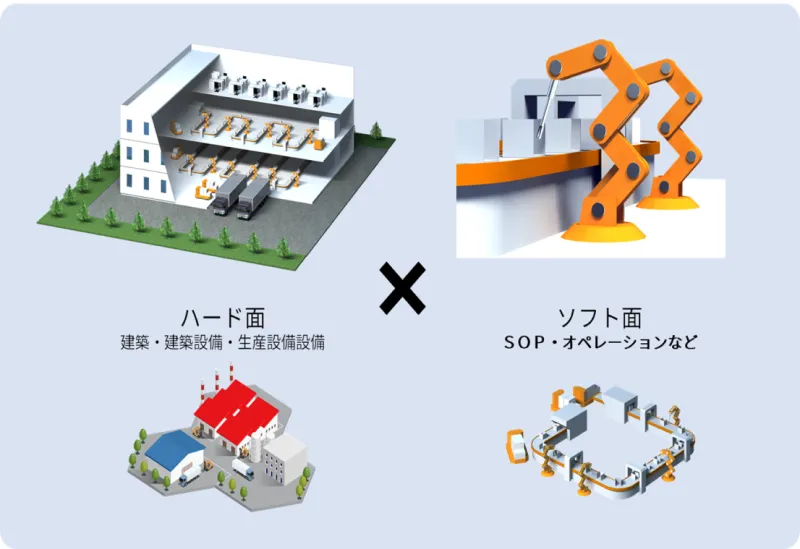
様々な分野での工場建設を経験したプロジェクトマネージャー、プロフェショナルエンジニアを擁しており、建物本体並びに製造支援設備はもちろんのこと、生産設備の購買サポート、製作管理、搬入計画の調整を含め、プロジェクトトータルでのスケジュール管理が可能です。

シーエムプラスの提供役務

事業構想
お客様のご要望をヒアリングし、主要機器リストやPFD・概念レイアウトなどの成果物を作成し、投資イメージを可視化します。
作成した成果物に基づき、概算投資金額を算出し、投資判断のサポートをいたします。(F/S、フィージビリスタディ)

基本計画
基本計画(概念設計)では、お客様のご要求・ご要望を打合せにてまとめ、ユーザー要求概要書(URB)として文書化いたします。また、URBの内容に基づきプロジェクト概算コストを算出いたします。

基本設計
基本設計では、URBの内容に基づき、効果的な引き合いができるように必要な図面・仕様書を作成していきます。特にプロセス設計では、プラント設計で必要となるPFD・P&ID・データシート・タイムスケジュール(OTS)・機器仕様書を作成いたします。また、施設の設計・建設に関連する法規基準や官庁申請、環境条件などを整理し、プロジェクトのマスタースケジュールや全体遂行計画の設定をサポートし、所轄官庁や電力・ユーティリティ供給会社等との事前調整の準備やサポートを行います。

見積引合い
見積引合い段階では、プロジェクトの特性に合わせた最適な遂行体制を構築するため、発注区分・役務区分を検討し、その内容を踏まえた引合仕様書・調達仕様書を作成して、施工会社へ引合を行います。施工会社から提示された見積・提案書に対し、技術評価・見積評価を行い報告書として纏めることで、お客様による施工会社選定のサポートを行います。

詳細設計・製作管理
詳細設計・製作段階では、施工会社や生産機器サプライヤーがURBや基本設計図書、各種レギュレーションを反映して設計を行っているか、スケジュール通り進捗しているかの観点で設計監理を行います。

施工・据付段階
施工・据付段階では、施工会社がURB・URSや実施設計図書、各種レギュレーションを反映して施工しているかの施工監理を行うことで、施設・設備の品質を管理いたします。
また、現場にコンストラクションマネージャーが常駐し、施工状況や工程、追加・増減管理をお客様の立場で行います。

試運転
高品質かつ効率的なクオリフィケーション遂行のため、計画段階から、バリデーションマスタープラン作成やリスクアセスメントのサポート、クオリフィケーション(DQ,IQ,OQ,PQ)実施のためのプロトコル作成を行い、遂行段階の支援までお客様の要望に合った形でサービスを提供し、お客様の負担を軽減します。
施設稼働
関連事例
関連コンテンツ
お役立ち情報
弊社の運営する情報発信サイト「GMP Platform」の記事もぜひご参考ください。

「医薬品工場建設のノウハウ」
医薬品工場建設プロジェクトの成功へのノウハウを集約。プロジェクトの仕組みづくりから、基本計画、基本設計~詳細設計、施工、バリデーションまで、各ステップの詳細とポイントを解説。