Sản phẩm y học tái tạo là gì?
Phân loại theo Đạo luật Dược phẩm và Thiết bị Y tế
Sản phẩm y học tái tạo sử dụng tế bào hoặc gen để điều trị hoặc phòng ngừa bệnh tật hoặc chấn thương. Phạm vi của các sản phẩm y học tái tạo được định nghĩa theo Đạo luật Dược phẩm và Thiết bị Y tế (thường được gọi là Đạo luật PMD) như sau:
- 1.Các sản phẩm trong đó tế bào từ người hoặc động vật đã được nuôi cấy hoặc xử lý theo cách khác, với mục đích:
a. Tái tạo, sửa chữa hoặc hình thành cấu trúc hoặc chức năng của cơ thể người hoặc động vật.
b. Điều trị hoặc phòng ngừa bệnh tật ở người hoặc động vật. - 2.Các sản phẩm dùng để điều trị bệnh tật ở người hoặc động vật liên quan đến việc đưa gen vào tế bào người hoặc động vật để biểu hiện chúng trong cơ thể.
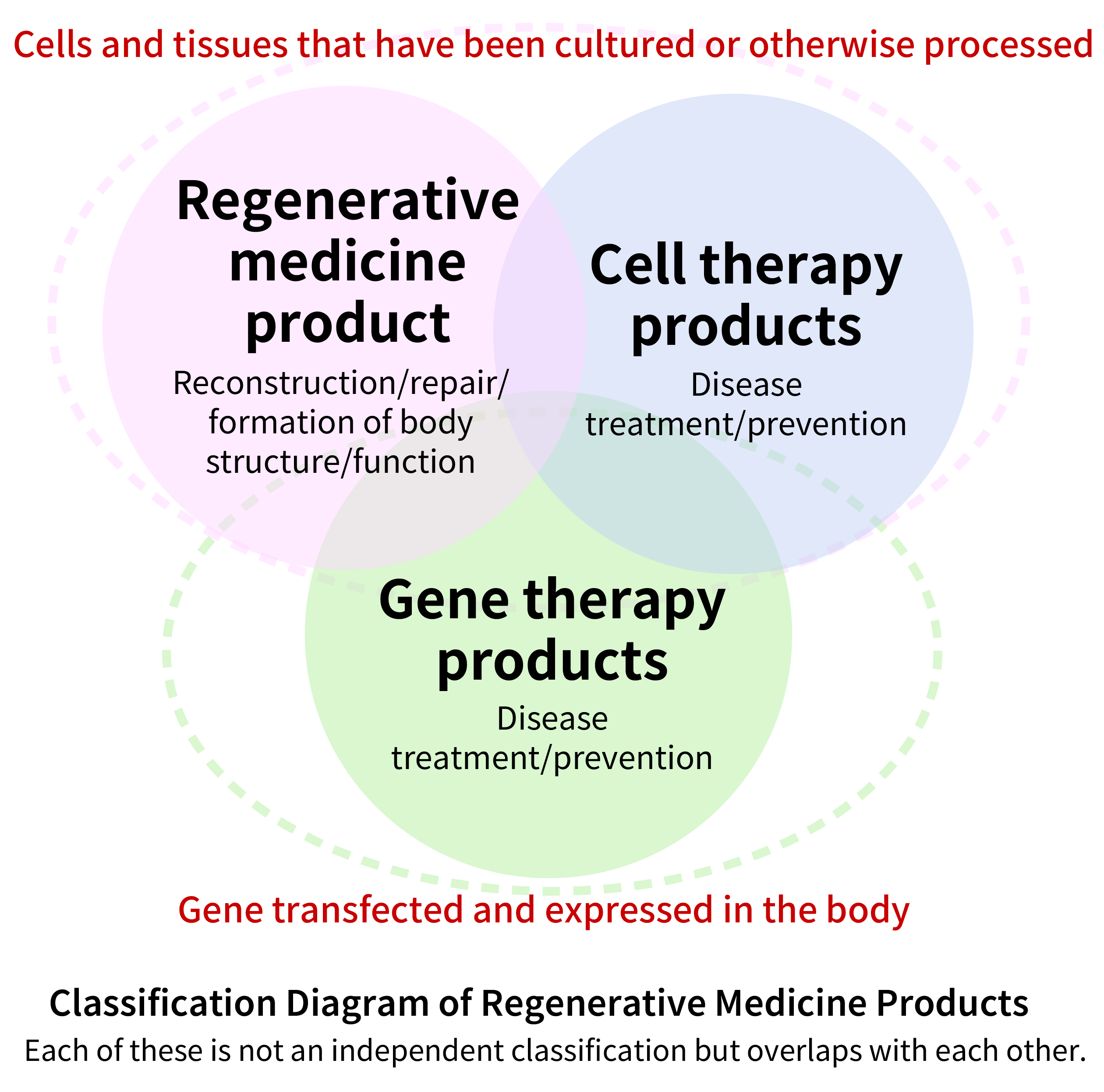
Các sản phẩm y học tái tạo được phân loại riêng biệt với thuốc và thiết bị y tế theo Đạo luật Dược phẩm và Thiết bị Y tế (thường được gọi là Đạo luật PMD). Vì các sản phẩm y học tái tạo liên quan đến việc sử dụng tế bào sống hoặc chính vi-rút làm sản phẩm, nên cần có quy trình sản xuất và kiểm soát chất lượng chuyên biệt khác với quy trình sản xuất và kiểm soát chất lượng đối với thuốc và thiết bị y tế.
Sự khác biệt giữa “Sản phẩm” và “Chăm sóc y tế” trong Y học tái tạo
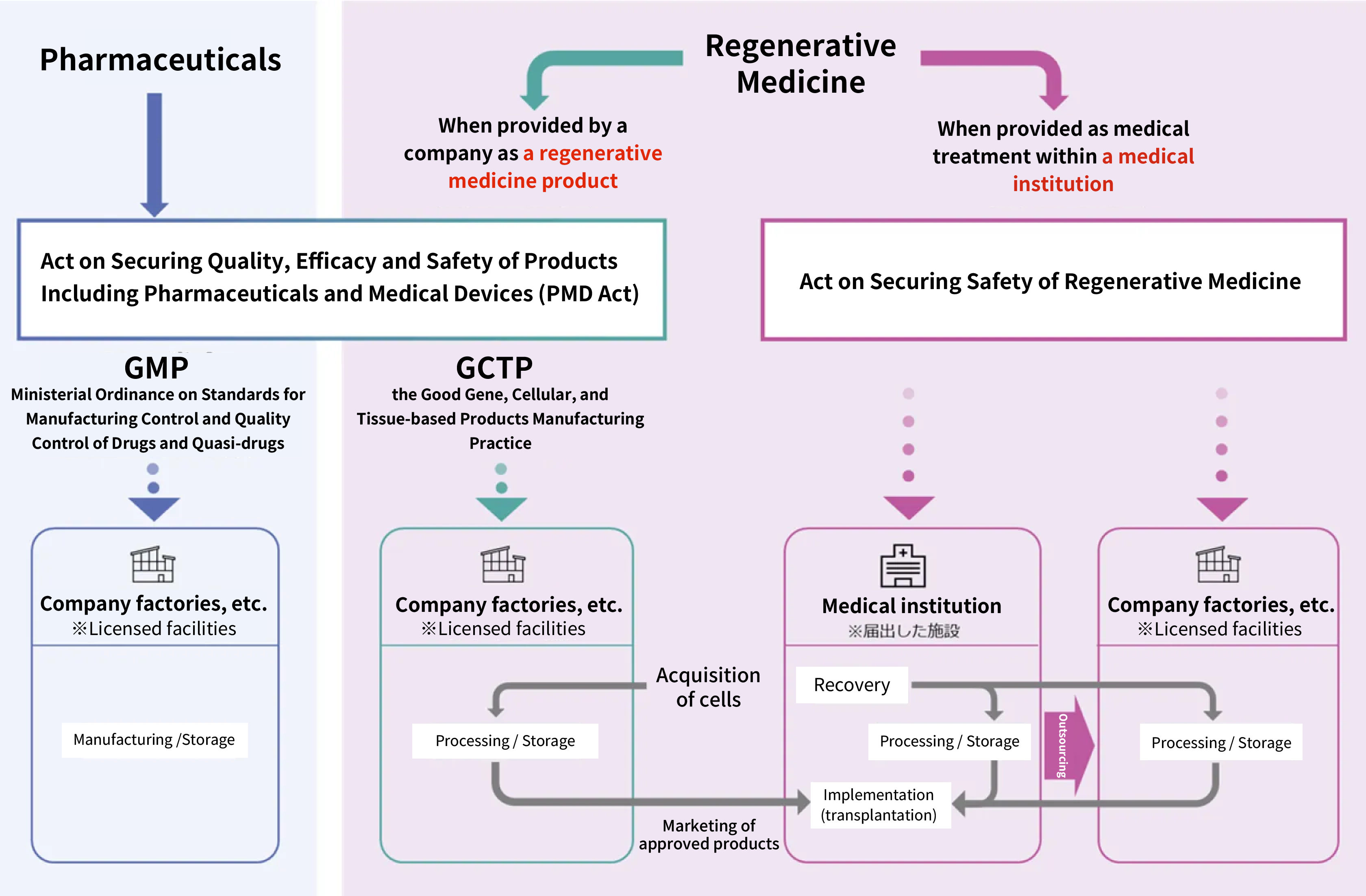
Trong y học tái tạo, các quy định áp dụng khác nhau tùy thuộc vào việc các sản phẩm y học tái tạo được cung cấp bởi các công ty hay dịch vụ chăm sóc y tế được cung cấp trong các cơ sở y tế. Sản phẩm trước phải tuân thủ Đạo luật Dược phẩm và Thiết bị y tế (Đạo luật PMD) và tuân thủ sắc lệnh Thực hành sản xuất các sản phẩm dựa trên gen, tế bào và mô tốt (GCTP), yêu cầu các cơ sở sản xuất phù hợp và kiểm soát chất lượng và sản xuất nghiêm ngặt. Mặt khác, sản phẩm sau phải tuân theo Đạo luật về Đảm bảo an toàn của Y học tái tạo, theo đó phải tiến hành nghiên cứu lâm sàng hoặc hành nghề y tư nhân.
Hỗ trợ của CM Plus cho các sản phẩm y học tái tạo
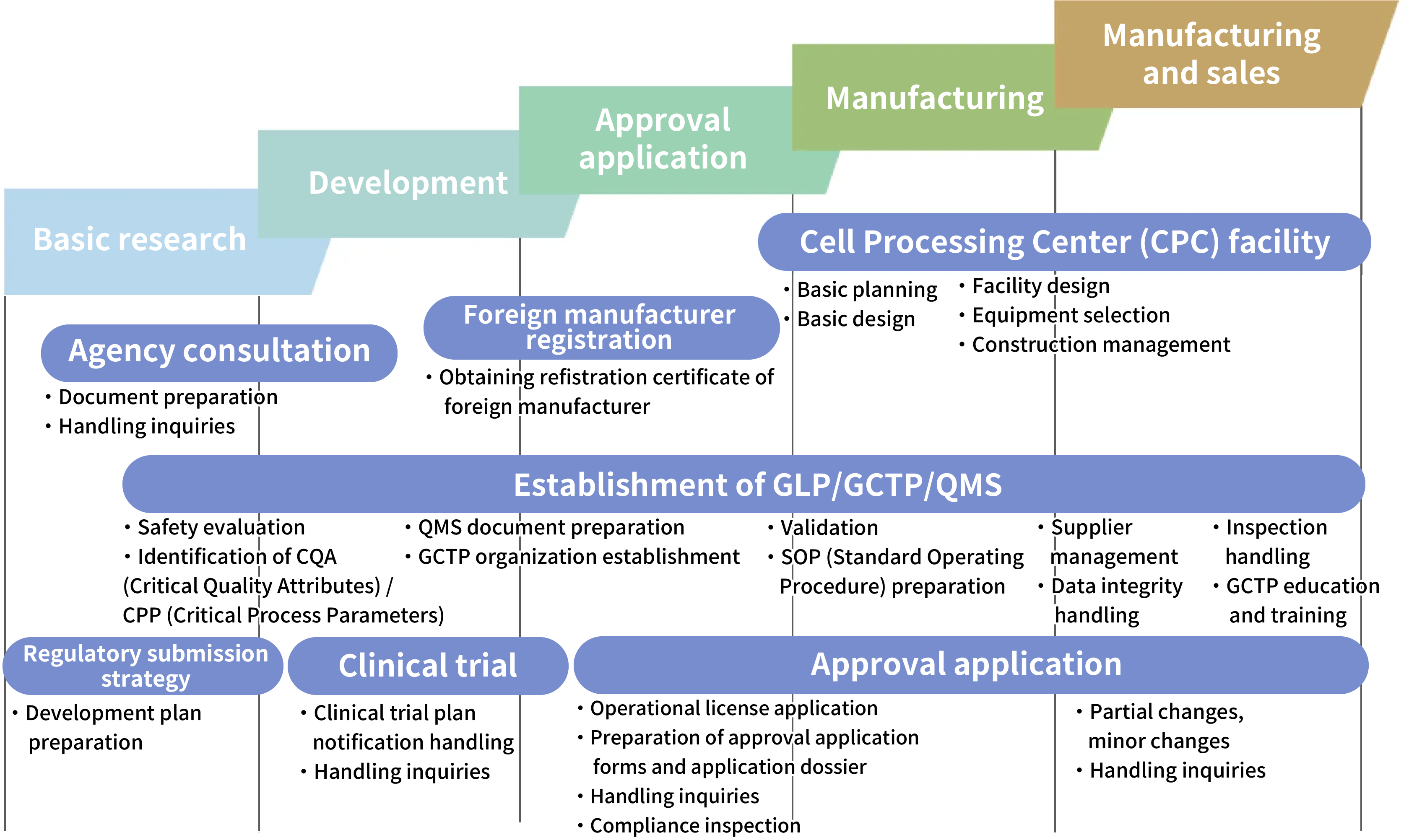
Các bước từ phát triển đến sản xuất và bán các sản phẩm y học tái tạo, v.v.
CM Plus hỗ trợ khách hàng của chúng tôi trong mọi giai đoạn, từ nghiên cứu cơ bản đến sau khi tiếp thị các sản phẩm y học tái tạo, v.v.
CM Plus có thể hỗ trợ nếu bạn muốn:
- Cân nhắc tham gia ngành y học tái tạo từ một lĩnh vực khác.
- xây dựng một tổ chức tuân thủ GCTP.
- mở rộng quy mô thiết bị từ quy mô phòng thí nghiệm lên quy mô thương mại và cần hỗ trợ cho các quyết định lựa chọn thiết bị và thông số kỹ thuật.
- Soạn thảo tài liệu tuân thủ theo phương pháp tiếp cận dựa trên rủi ro mới nhất./li>
- tư vấn về việc nên sở hữu cơ sở CPC nội bộ hay thuê ngoài.
- thực hiện thẩm định và soạn thảo SOP cho sản xuất nhưng thiếu nguồn lực nội bộ.
- tiến hành phân tích GAP để kiểm tra xem cơ sở của bạn có đáp ứng các yêu cầu pháp lý mới nhất hay không.
- có người đi cùng bạn để tham vấn trước và kiểm tra với các cơ quan quản lý.
- huê phòng thí nghiệm và lắp đặt thiết bị, và cần lập kế hoạch bố trí tuân thủ GCTP, v.v.

Dịch vụ tư vấn Y học tái tạo CM Plus có thể làm gì
- CM Plus có các chuyên gia tư vấn trong nhiều lĩnh vực khác nhau. trong lĩnh vực y học tái tạo, chúng tôi có thể cung cấp các giải pháp trọn gói cho nhu cầu của bạn bằng cách tích hợp các dịch vụ tư vấn và kỹ thuật. cho dù đó là các chiến lược đệ trình theo quy định trong giai đoạn nghiên cứu và phát triển, cơ cấu tổ chức GCTP hay lập kế hoạch cơ sở CPC trong giai đoạn sản xuất, chúng tôi đều có chuyên môn để hỗ trợ bạn.
Dịch vụ trọn gói cho Y học tái tạo của CM Plus
Các chuyên gia tư vấn và kỹ sư y học tái tạo giàu kinh nghiệm của chúng tôi cung cấp các dịch vụ phù hợp với nhu cầu cụ thể của bạn.

Tư vấn QMS/GCTP
-Hỗ trợ xây dựng các tổ chức tuân thủ QMS và GCTP
-Hỗ trợ huấn luyện GCTP
-Hỗ trợ quản lý nhà cung cấp
-Phân tích GAP và hỗ trợ thanh tra tra

Tư vấn đăng ký
-Hỗ trợ lập kế hoạch phát triển
-Hỗ trợ nhiều cuộc tham vấn khác nhau với cơ quan Dược phẩm và thiết bị y tế (PMDA)
-Hỗ trợ xin giấy phép sản xuất và lưu hành/giấy phép của nhà sản xuất/chứng nhận của nhà sản xuất nước ngoài (bao gồm cả việc trả lời các yêu cầu)
-Chuẩn bị các đơn xin phê duyệt và các tài liệu liên quan

Hỗ trợ xây dựng/chẩn đoán cơ sở và thiết bị
-Hỗ trợ thiết kế cơ sở bao gồm các kế hoạch cơ bản và thiết kế cơ sở cho các kế hoạch xây dựng cơ sở GPC
-Hỗ trợ lựa chọn thiết bị và soạn thảo thông số kỹ thuật khi đưa thiết bị sản xuất vào sử dụng
-Quản lý xây dựng trong quá trình xây dựng cơ sở CPC

Hỗ trợ Thẩm định
-Hỗ trợ soạn thảo tài liệu thẩm định khi giới thiệu thiết bị
-Soạn thảo các SOP khác nhau
-Nhiệm vụ quản lý thẩm định

Hỗ trợ đa ngôn ngữ
-Hỗ trợ các dự án xây dựng nhà máy đa quốc gia
-Hỗ trợ xin chứng nhận nhà sản xuất nước ngoài
-Cử phiên dịch viên cho cuộc thanh tra đa quốc gia
-Hỗ trợ Chuẩn bị tài liệu tiếng Anh
Ví dụ về Giải quyết Mối quan tâm của Bạn ① ①
(Dành cho các Công ty Y học Tái tạo)

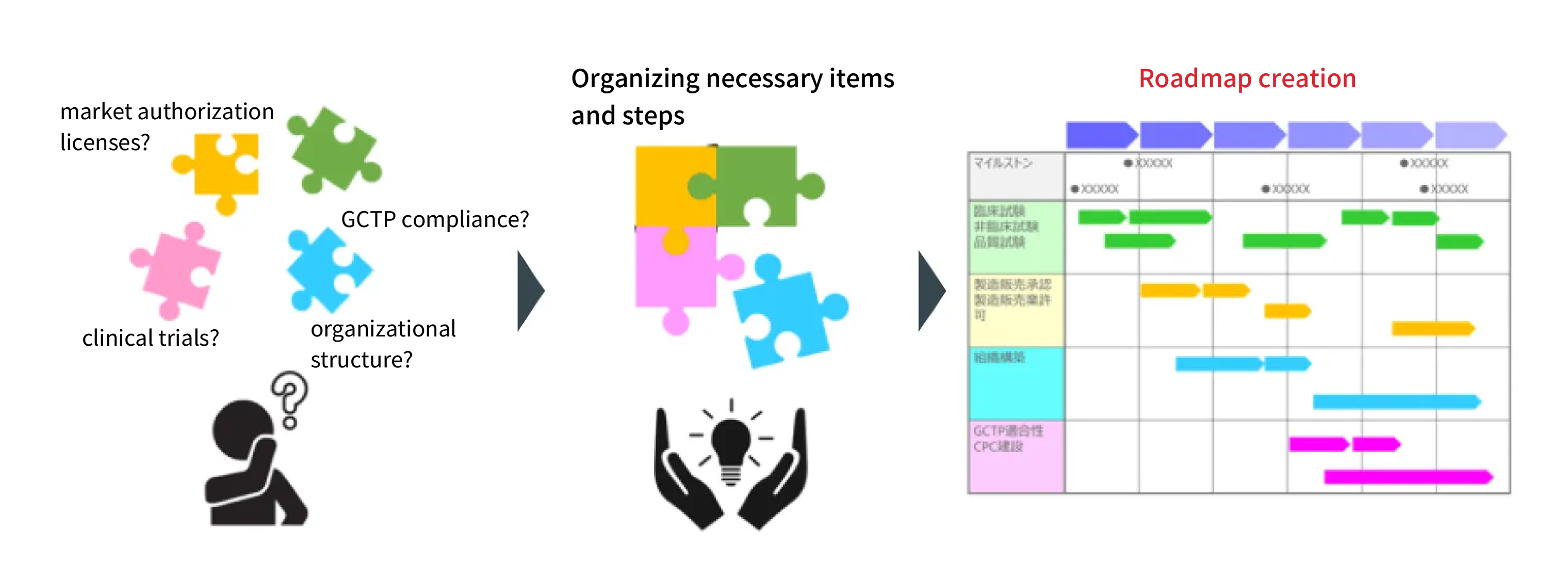
Chúng tôi đang khởi nghiệp kinh doanh y học tái tạo. Chúng tôi có một lịch trình sơ bộ, nhưng chúng tôi không biết bắt đầu từ đâu khi nói đến việc xin giấy phép ủy quyền, giấy phép sản xuất và lưu hành, xác nhận tuân thủ GCTP và xây dựng cơ cấu tổ chức.
Đối với những khách hàng có những mối quan tâm như vậy, CM Plus có thể cung cấp các hỗ trợ sau:


Soạn thảo Lộ trình cho Doanh nghiệp Y học Tái tạo và Kế hoạch Phát triển
Khi khởi nghiệp kinh doanh y học tái tạo, điều quan trọng là phải có một lộ trình được thiết kế tốt (lịch trình tổng thể) bao gồm toàn diện tất cả các quy trình và cuộc điều tra cần thiết theo một trình tự được lên kế hoạch cẩn thận. Việc tạo ra lộ trình này đòi hỏi trình độ chuyên môn và kinh nghiệm cao, do đó, sự tham gia của các chuyên gia có kiến thức về đăng ký, QMS và kinh nghiệm phát triển trong dược phẩm và y học tái tạo là điều cần thiết. CM Plus có nhiều cố vấn chuyên về lĩnh vực y học tái tạo, nộp hồ sơ đăng ký và xây dựng QMS. Chúng tôi có thể hỗ trợ bạn trong việc tổ chức từng bước – từ nghiên cứu cơ bản, thử nghiệm phi lâm sàng, thử nghiệm lâm sàng, thử nghiệm chất lượng, cấp phép ủy quyền, giấy phép sản xuất và tiếp thị, tuân thủ GCTP và chứng nhận của nhà sản xuất nước ngoài – cũng như trong việc soạn thảo và lập kế hoạch lộ trình của bạn

Ví dụ về Giải quyết Mối quan tâm của Bạn ②
((Dành cho Nhà sản xuất Thiết bị và Nhà sản xuất Thuốc thử Cân nhắc Tham gia Ngành Y học Tái tạo))

Chúng tôi muốn quảng bá sản phẩm của bạn đến các công ty y học tái tạo, nhưng chúng tôi thiếu kiến thức về GCTP và không tự tin trong việc phản hồi các cuộc thanh tra nhà cung cấp từ các công ty y học tái tạo.


Huấn luyện GCTP, Xây dựng Cấu trúc Tổ chức và Thanh tra Giả định Nhà cung cấp
Trong lĩnh vực y học tái tạo, cần phải tuân thủ các quy định của GCTP. CM Plus có thể cung cấp hỗ trợ huấn luyện GCTP và tư vấn về cấu trúc tổ chức tuân thủ các quy định của GCTP cho các nhà sản xuất thiết bị và nhà sản xuất thuốc thử tham gia vào ngành y học tái tạo. Chúng tôi cũng cung cấp các dịch vụ như tiến hành thanh tra nhà cung cấp giả định dựa trên các cuộc thanh tra của các công ty y học tái tạo, thực hiện kiểm tra tuân thủ GCTP và tiến hành phân tích GAP. Chúng tôi cung cấp dịch vụ trọn gói độc đáo của CM Plus, cung cấp tư vấn từ nhiều góc độ khác nhau bao gồm đặc điểm sản phẩm, GCTP, thiết bị, v.v.


Nội dung liên quan
Thông tin chi tiết của chuyên gia
Ngoài ra, vui lòng tham khảo các bài viết trên trang phổ biến thông tin của chúng tôi, “GMP Platform” do công ty chúng tôi điều hành.

Chuỗi bài “Y học tái tạo trong thực hành lâm sàng”

Chuỗi bài “Suy nghĩ về đảm bảo chất lượng cho Y học tái tạo và các sản phẩm liên quan”
Chuỗi bài “Cách tạo tài liệu sản xuất cho các kỹ sư trẻ trong Y học tái tạo”
Tổ chức “Triển lãm sản phẩm Y học tái tạo và Liệu pháp tế bào”
Nền tảng thông tin khoa học sự sống “iVEXL” của chúng tôi sẽ tổ chức “Triển lãm sản phẩm Y học tái tạo và Liệu pháp tế bào”. Vui lòng ghé thăm và thu thập thông tin.

Nhằm mục đích ứng dụng thực tế các sản phẩm y học tái tạo và liệu pháp tế bào, chúng tôi sẽ tập hợp các công nghệ và dịch vụ mới nhất từ nhiều công ty khác nhau, bao gồm các dịch vụ theo hợp đồng như nuôi cấy tế bào, thiết bị và dụng cụ, cũng như các giải pháp lưu trữ và vận chuyển.