Bạn có những mong muốn gì về việc nâng cao chất lượng sản phẩm?
- Chúng tôi muốn chuẩn bị cho các cuộc thanh tra theo quy định.
- Chúng tôi muốn một đối tác có thể thúc đẩy cụ thể việc xây dựng/cải thiện các hệ thống chất lượng.
- Chúng tôi muốn loại bỏ những lo ngại về các vấn đề và rủi ro tiềm ẩn trong cơ sở sản xuất.
- Chúng tôi muốn nhân sự chịu trách nhiệm kiểm toán các nhà máy sản xuất và nhà cung cấp nguyên liệu thô của các nhà thầu bên ngoài.
- Chúng tôi muốn thiết lập hiệu quả một hệ thống chất lượng trong các lĩnh vực kinh doanh mới.

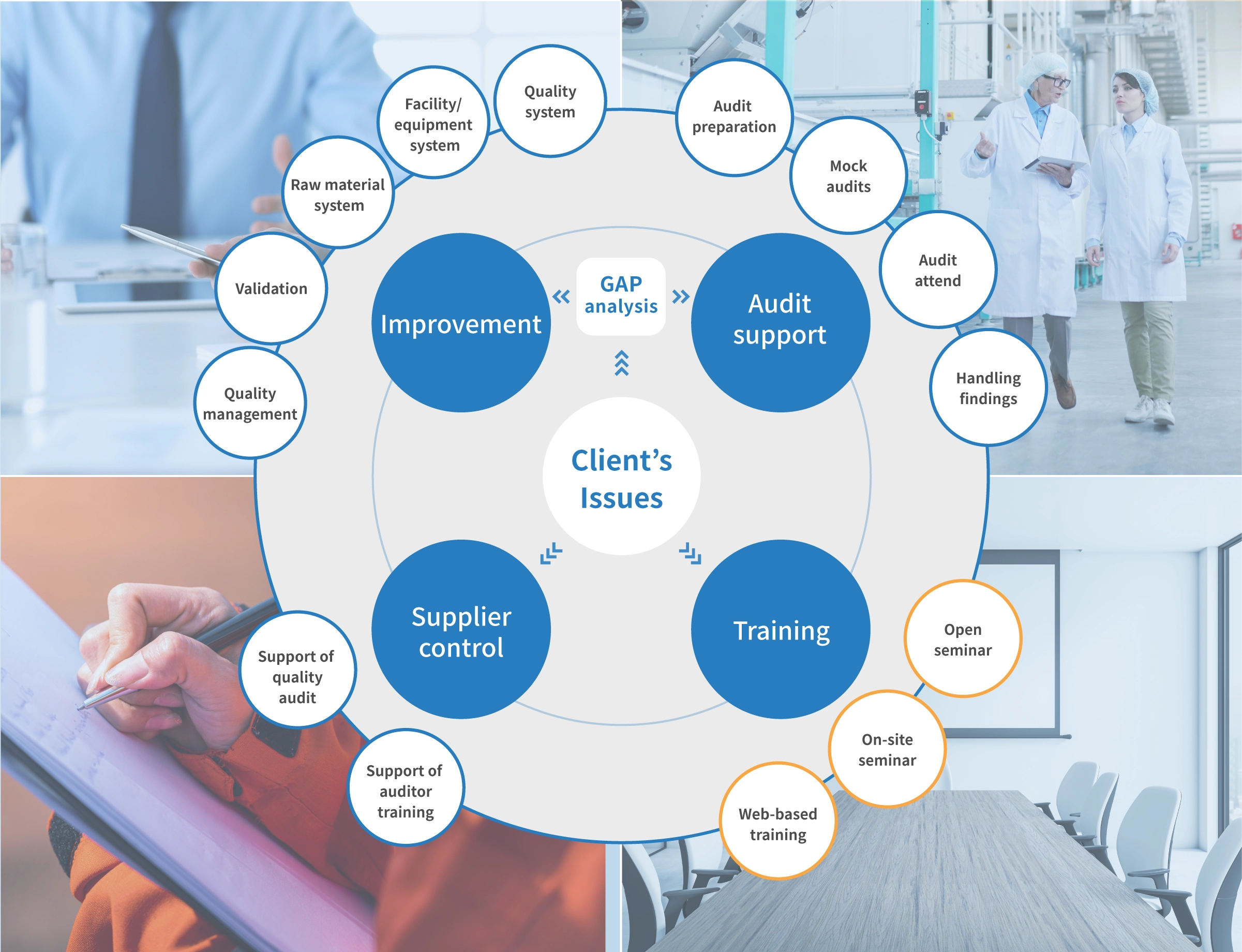
Với dịch vụ tư vấn GMDP của CM Plus, chúng tôi cung cấp các hỗ trợ sau cho
- Các cuộc thanh tra theo quy định như của FDA và PMDA:
- Các cuộc thanh tra giả định
- Đào tạo đối ứng thanh tra
- Hỗ trợ công tác hành chính (back office) trong suốt quá trình thanh tra
- Hỗ trợ xử lý các ý kiến, kết luận từ cuộc thanh tra
- Hỗ trợ cải thiện các vấn đề đã được xác định
- Phiên dịch trong các cuộc thanh tra quốc tế
- Các đề xuất toàn diện cho việc xây dựng và cải thiện PQS, quản lý lưu trữ nguyên liệu thô, cải thiện quy trình làm việc của cơ sở và cải thiện hoạt động tại chỗ. Điểm mạnh của Chúng tôi bao gồm đề xuất cải tiến cơ sở một cách suôn sẻ, được hỗ trợ bởi các cố vấn kỹ thuật nội bộ của Chúng tôi.
- Bằng cách tiến hành phân tích GAP, trước tiên Chúng tôi làm rõ những Điểm khác biệt (khoảng cách) giữa “trạng thái hiện tại” và “trạng thái mong muốn trong tương lai” của địa Điểm sản xuất. Chúng tôi xác định các rủi ro và vấn đề tiềm ẩn từ cả góc độ thiết bị/cơ sở và hệ thống chất lượng và đưa ra các đề xuất cải tiến.
- Các chuyên gia tư vấn giàu kinh nghiệm tiến hành kiểm toán chất lượng thay mặt cho bạn.
- Chúng tôi đào tạo Thanh tra viên GMP.
- Dựa trên kinh nghiệm sâu rộng, Chúng tôi hỗ trợ thiết lập các hệ thống chất lượng và chuẩn bị các quy trình phù hợp với quy mô nhân sự và các điều kiện khác.
ANgoài ra, CM Plus còn có các chuyên gia về quy định và xác nhận, cho phép chúng tôi cung cấp các buổi tư vấn trọn gói cho những vấn đề này.
Các chuyên gia tư vấn hàng đầu trong và ngoài Nhật Bản sẽ hỗ trợ bạn cải thiện chất lượng bằng cách cung cấp dịch vụ tư vấn cải tiến GMDP.
Hỗ trợ cải thiện
A:Hỗ trợ thiết lập/cải thiện hệ thống chất lượng của bạn
Về kiểm soát sản xuất/kiểm soát chất lượng, hỗ trợ chất lượng thuốc và liên quan đến tất cả các hoạt động từ B đến E được trình bày bên dưới, CM Plus cung cấp hỗ trợ cho việc thiết lập và cải tiến liên tục theo các hướng dẫn như “PIC/S GMP Guide Part I/II”. Chúng tôi đưa ra các đề xuất về cách thức thiết lập hệ thống tài liệu SOP dựa trên các chính sách chất lượng của bạn và hỗ trợ thiết lập các quy trình và hồ sơ bằng văn bản hỗ trợ chất lượng tại cơ sở sản xuất.
B:Đề xuất cải tiến hệ thống cơ sở vật chất và thiết bị
CM Plus xem xét cách bố trí, phân loại vệ sinh, luồng nhân sự và vật liệu theo GMP sau đó đưa ra đề xuất các biện pháp cải tiến.
C:Hỗ trợ thiết lập/cải thiện hệ thống nguyên liệu thô của bạn
CM Plus đưa ra đề xuất về cách cải thiện việc lựa chọn và quản lý nhà cung cấp, quản lý kho lưu trữ nguyên liệu thô và sản phẩm, quản lý việc vận chuyển vật liệu vào/ra khỏi kho và phân phối.
D:Hỗ trợ thiết lập/cải thiện hệ thống kiểm soát phòng thí nghiệm
CM Plus hỗ trợ thiết lập hệ thống kiểm soát toàn bộ phòng thí nghiệm bao gồm kiểm soát mẫu, chuẩn tham chiếu và thuốc thử, đủ điều kiện, bảo trì và hiệu chuẩn các thiết bị phòng thí nghiệm, xác nhận phương pháp phân tích và đảm bảo tính toàn vẹn của dữ liệu.
E:Hỗ trợ các hoạt động thẩm định
Sau khi công bố “Hướng dẫn của FDA” năm 2011 và sửa đổi “Phụ lục 15 của Hướng dẫn GMP PIC/S” năm 2015, khái niệm xác nhận quy trình đã thay đổi mạnh mẽ và được định vị là các hoạt động liên tục cần thực hiện trong suốt vòng đời sản phẩm. CM Plus xem xét dữ liệu CMC của khách hàng và đề xuất các phương pháp tiếp cận hiệu quả để bạn có thể đảm bảo khả năng truy xuất nguồn gốc phù hợp đối với dữ liệu bằng chứng được tích lũy trong quá trình phát triển sản phẩm của mình. Ngoài ra, chúng tôi sẽ hỗ trợ khách hàng phát triển cải tiến liên tục dựa trên các đánh giá chất lượng sản phẩm.
-
Để thẩm định nhà máy sản xuất và thiết bị kiến trúc, vui lòng xem tại đây.
Hỗ trợ thanh tra
CM Plus tiến hành các cuộc thanh tra giả lập (mock audits) với đội ngũ kiểm tra viên giàu kinh nghiệm, từng thực hiện thanh tra tại Nhật Bản, Hoa Kỳ, châu Âu hoặc từng là thanh tra viên tại các cơ quan quản lý. Dựa trên kết quả của các cuộc thanh tra giả lập này, chúng tôi cung cấp cho khách hàng những lời khuyên và đề xuất cải tiến phù hợp với tình trạng chuẩn bị hiện tại của họ.Bên cạnh đó, chúng tôi còn hỗ trợ phía hậu trường trong suốt quá trình thanh tra thực tế và hỗ trợ xử lý các ý kiến, kết luận sau thanh tra.
- Các cuộc thanh tra giả lập do đội ngũ kiểm tra viên của chúng tôi thực hiện, những người có kinh nghiệm thanh tra tại Nhật Bản, Hoa Kỳ, châu Âu hoặc từng là thanh tra viên tại các cơ quan quản lý (mô phỏng được tiến hành theo đúng quy trình như các cuộc thanh tra thực tế).
- Phân tích năng lực hiện tại của khách hàng về công tác thanh tra GMP và đề xuất các giải pháp cải thiện.
- Đào tạo cho nhân sự phụ trách phản hồi trong thanh tra
- Hỗ trợ chuẩn bị nhiều tài liệu khác nhau và họp với cơ quan có thẩm quyền
*Ví dụ về hỗ trợ của chúng tôi cho các cuộc thanh tra của FDA: hỗ trợ chuẩn bị các gói cho các cuộc họp sơ bộ (Cuộc họp loại C) và tham dự các cuộc họp - Tư vấn hỗ trợ phía hậu trường trong quá trình thanh tra về việc chuẩn bị tài liệu và cách trả lời
- Hỗ trợ soạn thảo các thỏa thuận bằng văn bản nhằm thực hiện các cải tiến theo kết luận từ cuộc thanh tra và chuẩn bị các phản hồi bằng văn bản
Hỗ trợ Đào tạo/Huấn luyện GMDP (GMP & GDP)
Đối với các hoạt động sản xuất thuốc, việc liên tục đào tạo hiệu quả cho nhân viên về GMDP và giúp họ hiểu đúng về GMDP là rất quan trọng. CM Plus cung cấp cho bạn các khóa học “học trực tuyến (e-Learning)” và “hội thảo mở (open seminars)” dành cho cá nhân, cũng như “hội thảo tại chỗ (on-site seminars)” dành cho tổ chức.
Để biết thêm chi tiết về e-learning, hội thảo mở và hội thảo tại chỗ, vui lòng xem mục “Hỗ trợ Đào tạo/Huấn luyện” trên website của chúng tôi.
Đường link dưới đây sẽ dẫn bạn đến GMP Platform do chúng tôi vận hành.
Hỗ trợ kiểm soát nhà cung cấp
Các chuyên gia tư vấn giàu kinh nghiệm hỗ trợ thanh tra chất lượng (thanh tra nhà cung cấp)
Chúng tôi cũng có thể hỗ trợ thanh tra các nhà sản xuất công thức thuốc/API và các nhà cung cấp nguyên liệu thô/vật liệu đóng gói và dán nhãn.
A: Hỗ trợ thực hiện và phân công thanh tra chất lượng trong và ngoài nước
CM Plus tiến hành thanh tra chất lượng cùng với bạn hoặc thay mặt bạn cho các nhà sản xuất theo hợp đồng và nhà cung cấp nguyên liệu và vật liệu. Các chuyên gia của chúng tôi, với kinh nghiệm tư vấn sâu rộng trong nước và quốc tế, sẽ xử lý các nhiệm vụ này. Chúng tôi hỗ trợ thanh tra không chỉ cho các cơ sở sản xuất trong nước mà còn cho các cơ sở sản xuất ở nước ngoài.
B: Hỗ trợ đào tạo thanh tra viên
CM Plus cung cấp chương trình đào tạo giáo dục cho người mới bắt đầu, người mới đến và giám sát đào tạo để hỗ trợ phát triển và cấp chứng chỉ nội bộ cho các thanh tra viên. Đối với các công ty đang thiếu hụt nhân sự thanh tra, “Chương trình đào tạo thanh tra viên GMP” do chúng tôi tổ chức thường xuyên đã được đón nhận nồng nhiệt. Chương trình này sử dụng các tài liệu gốc, được thiết kế có hệ thống do các giảng viên giàu kinh nghiệm biên soạn và bao gồm các bài tập thực hành (đóng vai) mô phỏng các tình huống thực tế một cách sát nhất có thể.
Để biết thông tin về Chương trình đào tạo thanh tra viên, vui lòng xem mục “Hỗ trợ Đào tạo/ Huấn luyện”.
Đường link dưới đây sẽ dẫn bạn đến GMP Platform do chúng tôi vận hành.
Dịch vụ khác
A: GMP cho các sản phẩm thuốc nghiên cứu (IMP) (IMPs)
CM Plus hỗ trợ xây dựng hệ thống cGMP cho các sản phẩm thuốc nghiên cứu và thiết lập Quy trình vận hành chuẩn (SOP). Điều này bao gồm các tình huống mà các công ty công nghệ sinh học và các công ty khác thuê ngoài hoàn toàn việc sản xuất các hợp chất đang được nghiên cứu khi chúng chuyển sang giai đoạn phát triển.
B: Hỗ trợ hoạt động GQP
Liên quan đến GQP (Thực hành chất lượng tốt), vốn là quy định đặc biệt của Nhật Bản, các cố vấn giàu kinh nghiệm của chúng tôi hỗ trợ thiết lập hệ thống GQP và cải thiện SOP.
Quy trình tư vấn
Họp trực tuyến hoặc tại chỗ
Sau khi lắng nghe yêu cầu của bạn, chúng tôi sẽ giới thiệu các dịch vụ chúng tôi có thể cung cấp. Dựa trên thông tin thu thập được, chúng tôi sẽ gửi báo giá và bảng thông số kỹ thuật sau. Nếu cần thiết, một thỏa thuận bảo mật sẽ được ký kết trước cuộc họp.
Đặt hàng và Hợp đồng
Nếu bạn đồng ý đặt hàng dịch vụ và các điều khoản báo giá của chúng tôi, chúng tôi sẽ (1) phát hành lệnh mua hàng có thỏa thuận bảo mật hoặc (2) ký kết thỏa thuận ký gửi kinh doanh bao gồm cả bảo mật.
Triển khai tư vấn
Chúng tôi sẽ tiến hành tư vấn thực tế, chẳng hạn như phân tích GAP, hỗ trợ cải tiến và đại diện thanh tra, thông qua các chuyến thăm thực tế hoặc trực tuyến.
Nộp báo cáo và tài liệu
Dựa trên thỏa thuận với khách hàng, chúng tôi sẽ gửi hồ sơ tư vấn, báo cáo thanh tra và các tài liệu liên quan khác.