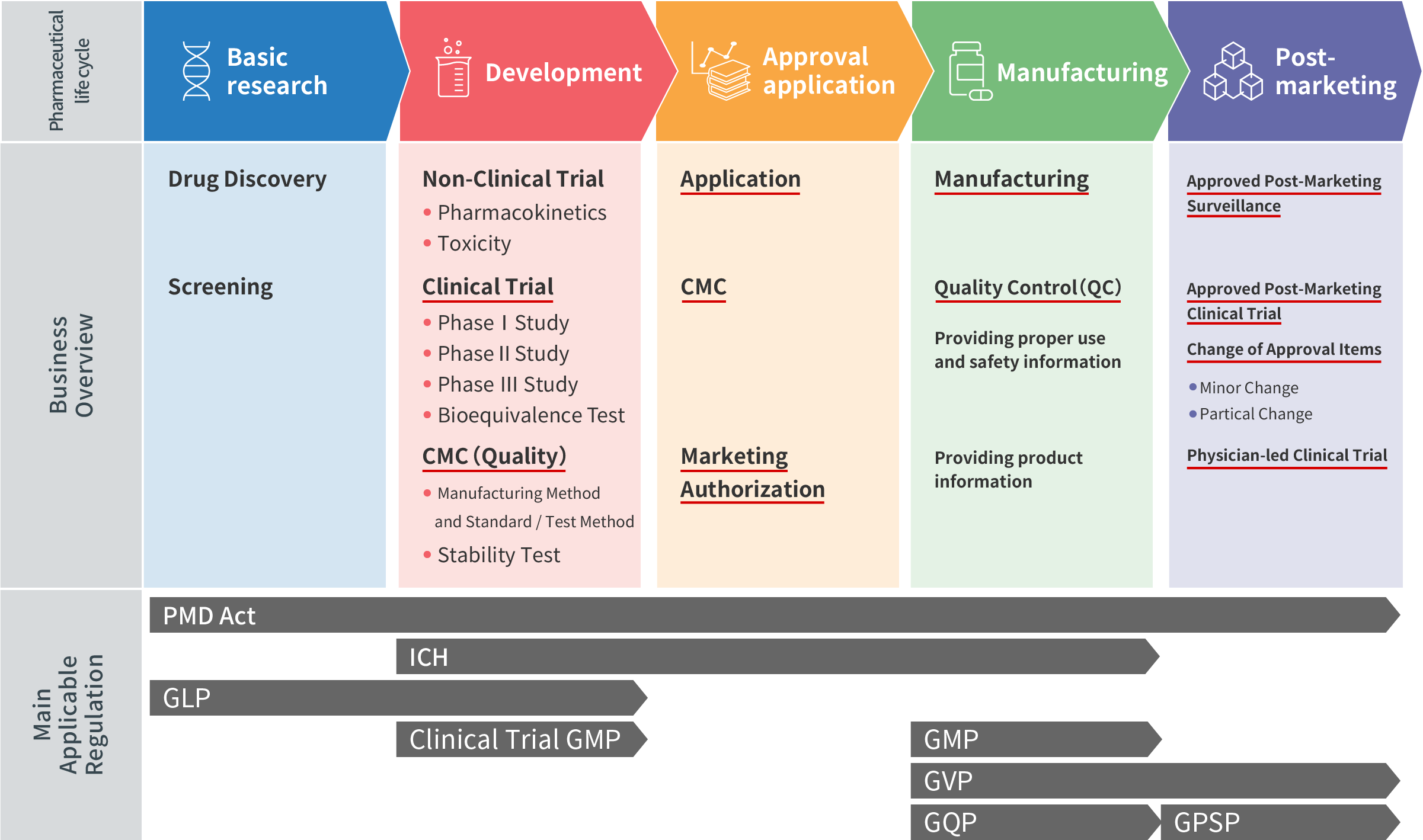
Siklus hidup farmasi dan tugas di setiap langkahnya
Setiap langkah dalam siklus hidup farmasi melibatkan tugas-tugas berikut:
- * Garis bawah merah menunjukkan cakupan layanan konsultasi regulasi CM Plus.
Konsultasi Urusan Regulasi Farmasi dari CM Plus
Para ahli kami menawarkan layanan konsultasi urusan regulasi farmasi dengan pengalaman praktis yang melimpah di industri ini untuk memenuhi kebutuhan pelanggan kami.
- Strategi Aplikasi Regulasi
- Membangun Sistem Internal seperti GQP / GVP
- Berbagai Konsultasi dengan Badan Farmasi dan Alat Kesehatan (PMDA)
- Dukungan untuk Lisensi Bisnis Manufaktur/Pemasaran untuk Produk Farmasi, dll./ Lisensi Bisnis Manufaktur/ Aplikasi untuk Akreditasi Produsen Asing (termasuk Dukungan untuk Respons Pertanyaan)
- Dukungan Bisnis untuk Membuat Formulir Aplikasi Persetujuan dan Materi Aplikasi
- Dukungan Bisnis untuk Perubahan Sebagian, perubahan kecil (termasuk dukungan untuk respon pertanyaan)
Pelanggan Mendapat Manfaat dari Konsultasi Urusan Regulasi Farmasi CM Plus
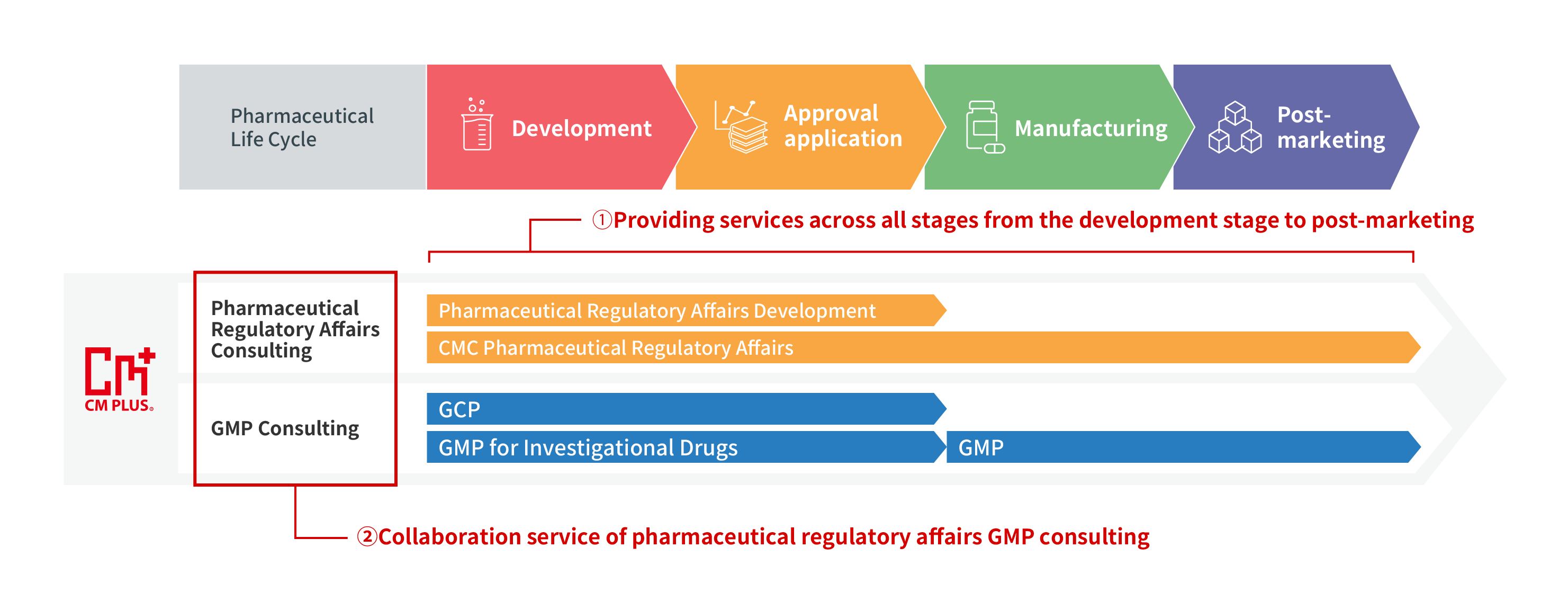
Layanan Konsultasi Urusan Regulasi di semua tahap, dari Pengembangan hingga Pasca Pemasaran
CM Plus menyediakan layanan konsultasi untuk pengembangan urusan regulasi, urusan regulasi CMC, dan urusan regulasi farmasi di semua tahap, mulai dari tahap pengembangan, pengajuan persetujuan, produksi, hingga pasca pemasaran. Kami dapat menangani obat baru, obat generik, obat yang sudah lama terdaftar (setelah masa pemeriksaan ulang), dan berbagai jenis obat.
Layanan Konsultasi Urusan Regulasi Bekerja sama dengan Layanan Konsultasi GMP.
CM Plus menyediakan dua layanan. Yang pertama adalah “layanan konsultasi GMP, dari perspektif departemen jaminan mutu QA dan manufaktur GMP” (dukungan di tempat). Yang kedua adalah “layanan konsultasi urusan regulasi farmasi, dari perspektif interpretasi regulasi dan prosedur dokumen” (kami menyediakan layanan konsultasi respons regulasi kepada otoritas regulasi, dari aplikasi hingga respons pertanyaan). Menggabungkan kedua layanan ini memungkinkan kami untuk menyediakan layanan konsultasi GMP, QA, dan regulasi kolaboratif yang lebih sesuai untuk lokasi..
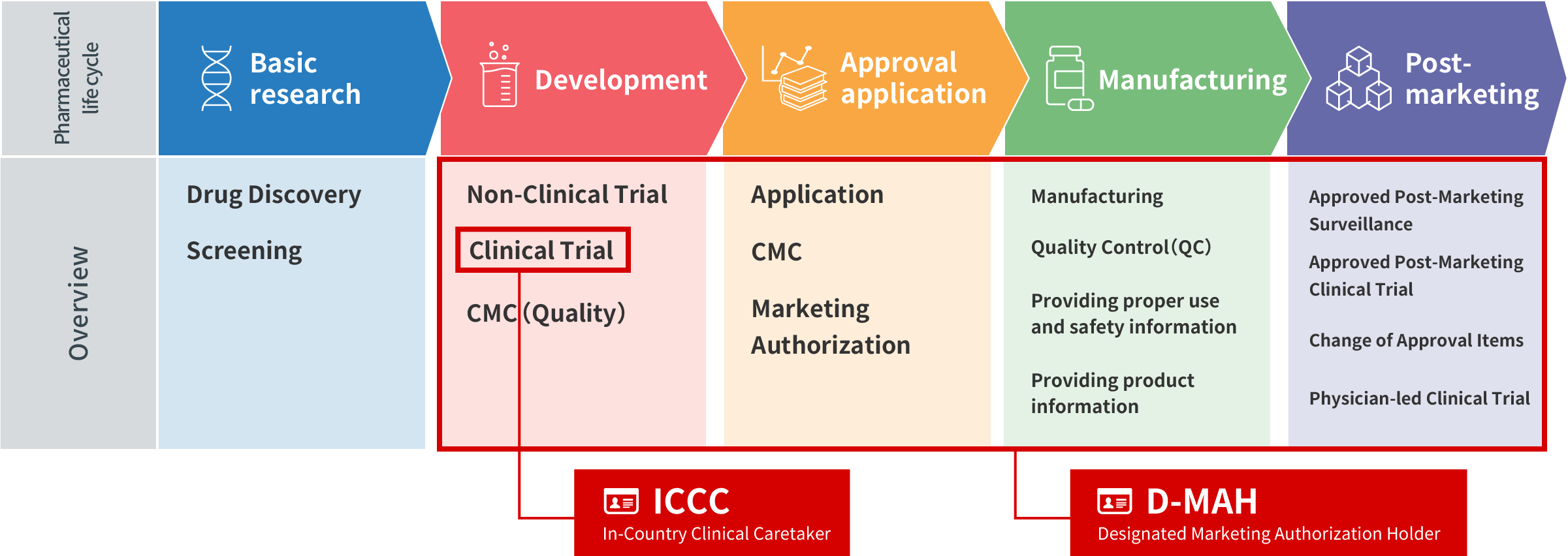
Pemegang Otorisasi Pemasaran Tertunjuk
dan Pengasuh Klinis Dalam Negeri
CM Plus telah memperoleh lisensi pemasaran kelas satu dan kelas dua untuk obat-obatan. Kami dapat ditunjuk sebagai Pemegang Otorisasi Pemasaran Tertunjuk (D-MAH) untuk perusahaan yang tidak memiliki perusahaan yang berdiri di Jepang. Kami juga menyediakan layanan dukungan apa pun untuk uji klinis di Jepang yang sesuai dengan Peraturan Menteri GCP Jepang sebagai Pengasuh Klinis Dalam Negeri (ICCC: Pasal 15 dalam Peraturan Menteri GCP) (peran sponsor di Jepang)
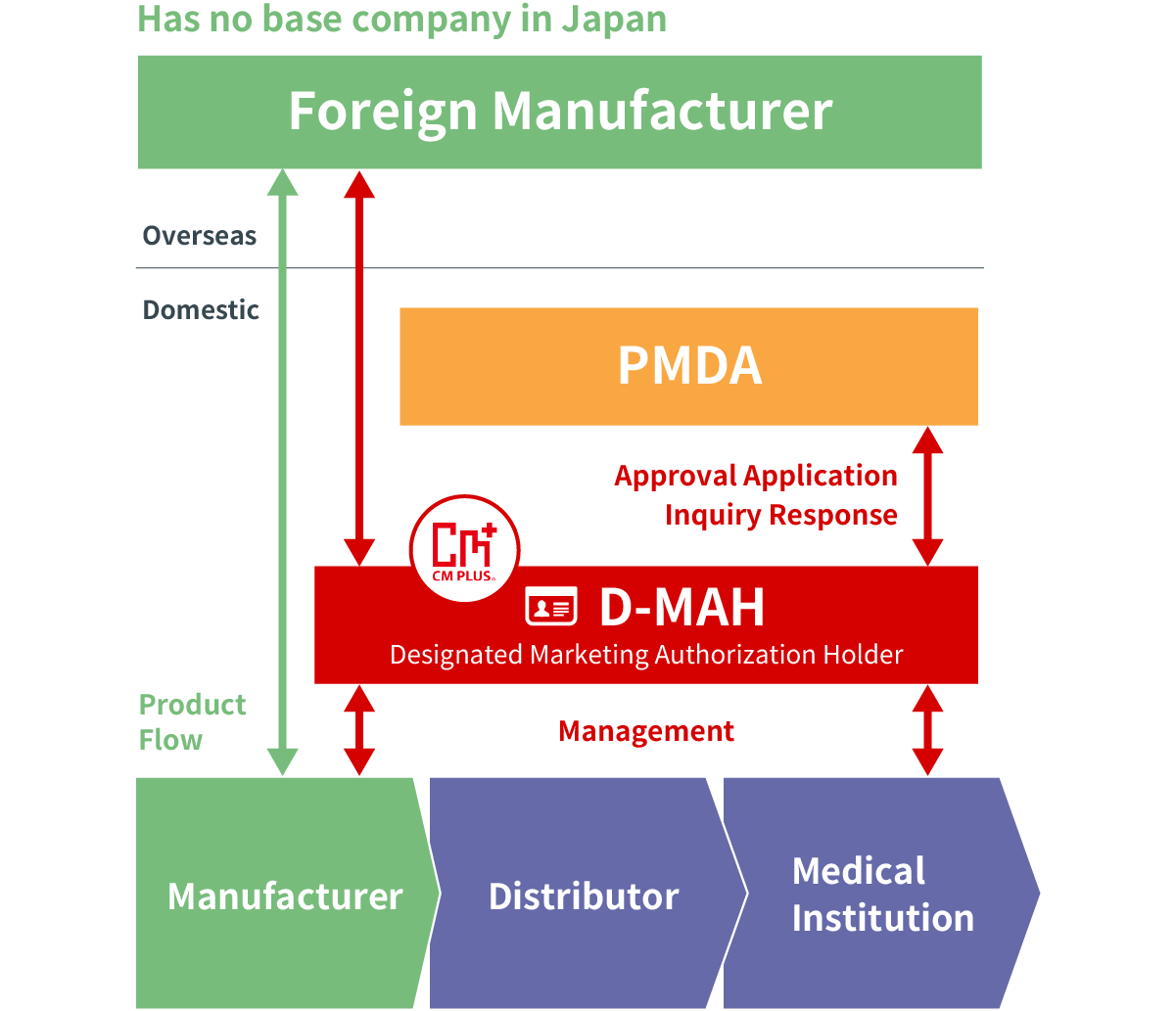
Layanan Pemegang Otorisasi Pemasaran Tertunjuk (D-MAH)
Layanan ini memungkinkan produsen asing untuk memasuki pasar Jepang untuk produk farmasi secara sukarela.
Jika produsen asing tidak memiliki basis operasi bisnis di Jepang untuk penjualan obat-obatan dan alat kesehatan, maka perlu menunjuk satu pemegang lisensi bisnis manufaktur/pemasaran di Jepang.
CM Plus telah memperoleh lisensi pemasaran kelas satu dan kelas dua untuk obat-obatan. Kami akan menyediakan layanan sebagai Pemegang Otorisasi Pemasaran Tertunjuk (D-MAH) bagi produsen asing yang telah memasuki pasar Jepang dan mempertimbangkan untuk mengimpor dan menjual.
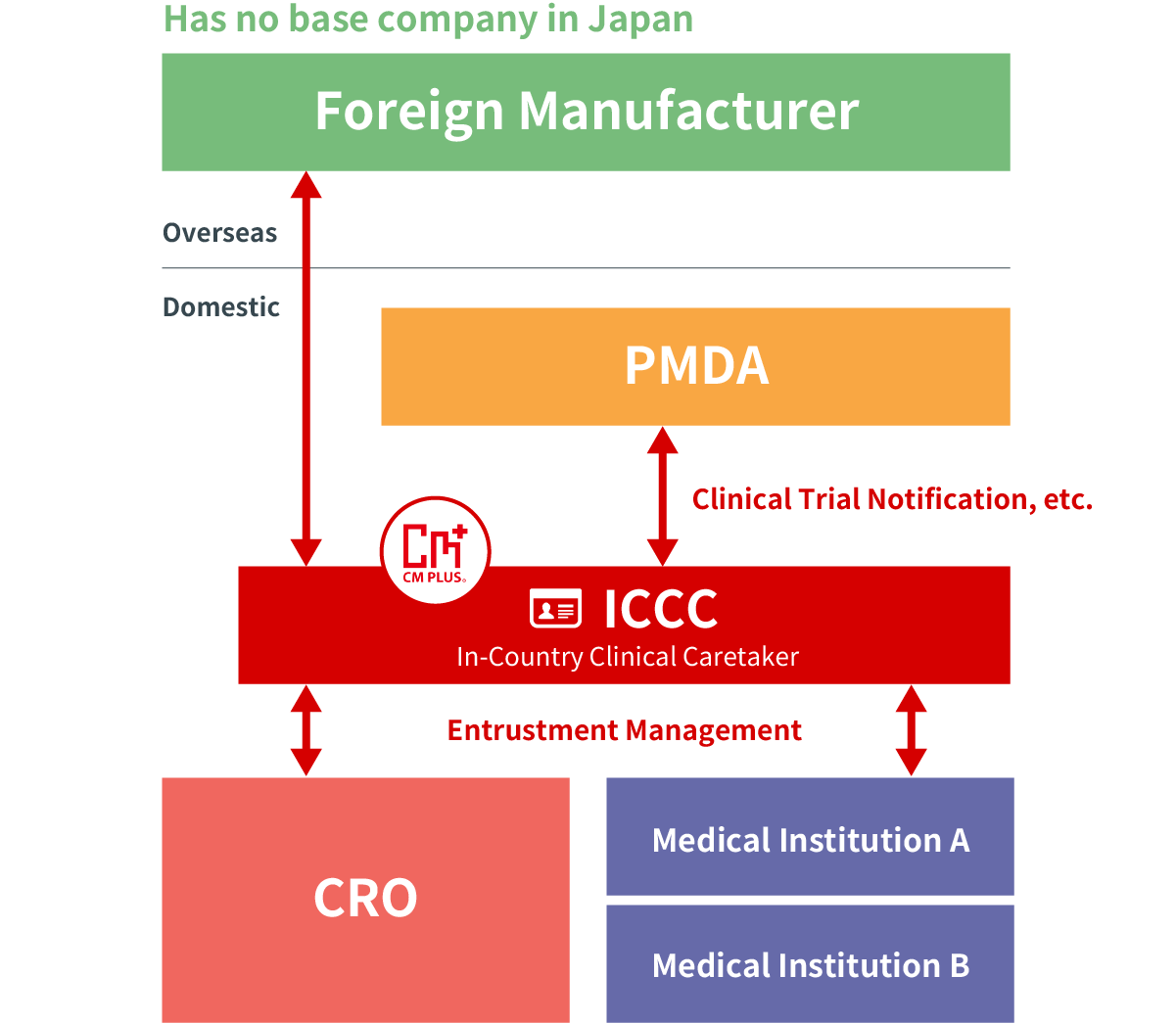
Layanan Perawat Klinis Dalam Negeri (ICCC)
Layanan ini memungkinkan uji klinis dilakukan di Jepang atas nama perusahaan farmasi luar negeri (perusahaan farmasi, usaha penemuan obat, dll.) tanpa badan hukum.
Ketika perusahaan tanpa badan hukum di Jepang melakukan uji klinis di Jepang, perlu untuk mencegah terjadinya atau penyebaran bahaya kesehatan yang disebabkan oleh obat yang diteliti. Diperlukan untuk menunjuk orang yang beralamat di Jepang sebagai orang yang dapat meminta uji klinis atas nama orang tersebut.
Sebagai mitra pengembangan klinis, CM Plus akan memainkan peran sponsor di Jepang (ICCC: Pasal 15 dalam Peraturan Menteri GCP) atas nama perusahaan farmasi tanpa basis bisnis di Jepang.
Apakah Anda memiliki masalah berikut?
Untuk Perusahaan Luar Negeri

Bahkan jika Kami tidak memiliki perusahaan basis bisnis di Jepang, dapatkah Kami memperoleh persetujuan Manufaktur/pemasaran produk farmasi tanpa memberikan lisensi kepada produk tersebut?


CM Plus telah memperoleh lisensi bisnis untuk lisensi pemasaran kelas satu dan kelas dua untuk farmasi. Penunjukan CM Plus sebagai Pemegang Otorisasi Pemasaran Tertunjuk (D-MAH) memungkinkan untuk mengajukan persetujuan khusus asing. Anda dapat menggunakannya untuk mengajukan persetujuan Pemasaran di Jepang.

Apakah mungkin untuk melakukan uji klinis di Jepang meskipun tidak ada perusahaan yang berbasis di Jepang?


Dengan menunjuk CM Plus sebagai In-Country Clinical Caretaker (ICCC), uji klinis dapat dilakukan di Jepang sesuai kebutuhan. Selain itu, kami memiliki staf dengan pengalaman yang melimpah dalam pengembangan dan pemasaran, dan CMP dapat mengusulkan sistem implementasi uji klinis (CRO, lembaga medis, lembaga pengujian) di Jepang.