Apa itu produk pengobatan regeneratif?
Klasifikasi berdasarkan Undang-Undang Farmasi dan Alat Kesehatan
Produk pengobatan regeneratif menggunakan sel atau gen untuk pengobatan atau pencegahan penyakit atau cedera. Cakupan produk pengobatan regeneratif yang ditetapkan berdasarkan Undang-Undang Farmasi dan Alat Kesehatan (umumnya dikenal sebagai Undang-Undang PMD) adalah sebagai berikut:
- 1.Produk yang selnya berasal dari manusia atau hewan yang telah dikulturkan atau diproses dengan cara lain, dengan tujuan:
a. Rekonstruksi, perbaikan, atau pembentukan struktur atau fungsi tubuh manusia atau hewan.
b. Pengobatan atau pencegahan penyakit pada manusia atau hewan. - 2.Produk yang ditujukan untuk pengobatan penyakit pada manusia atau hewan yang melibatkan pengenalan gen ke dalam sel manusia atau hewan untuk mengekspresikannya dalam tubuh.
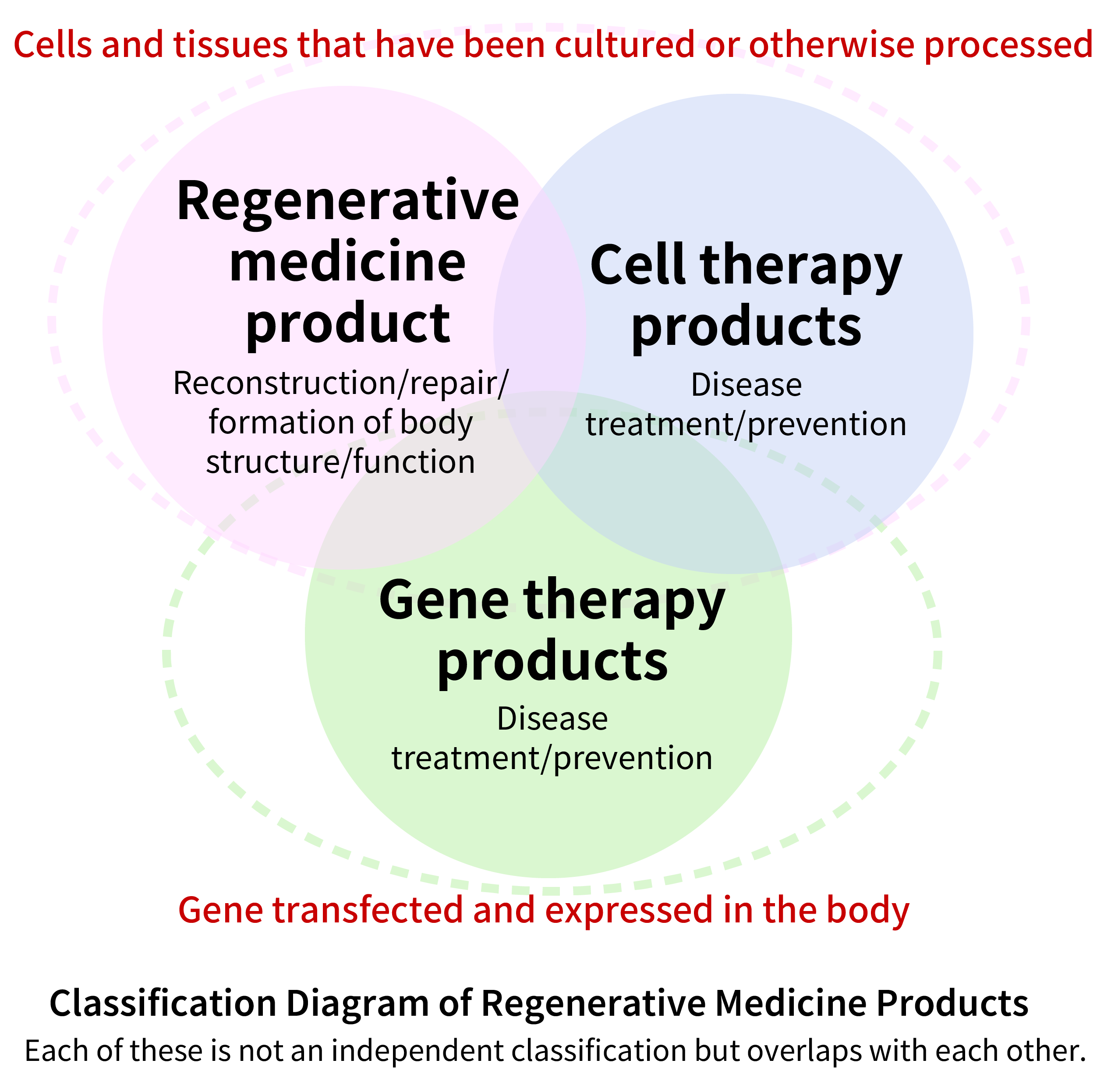
Produk pengobatan regeneratif diklasifikasikan secara terpisah dari obat-obatan dan alat kesehatan berdasarkan Undang-Undang Farmasi dan Alat Kesehatan (umumnya dikenal sebagai Undang-Undang PMD). Karena produk pengobatan regeneratif melibatkan penggunaan sel hidup atau virus itu sendiri sebagai produk, diperlukan produksi dan pengendalian mutu khusus yang berbeda dari obat-obatan dan alat kesehatan.
Perbedaan Antara “Produk” dan “Perawatan Medis” dalam Pengobatan Regeneratif
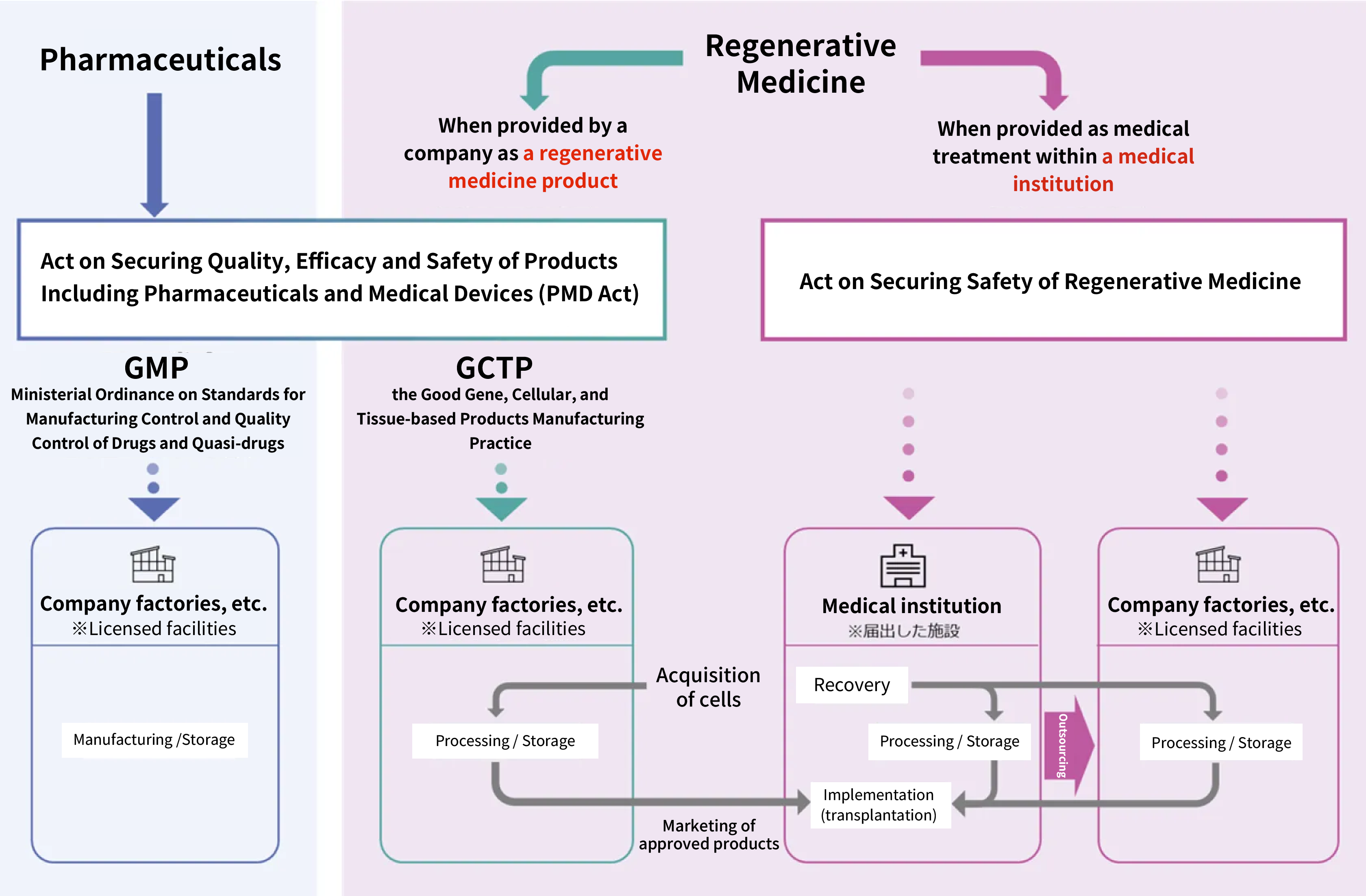
Dalam pengobatan regeneratif, peraturan yang berlaku berbeda-beda, tergantung pada apakah produk pengobatan regeneratif disediakan oleh perusahaan atau perawatan medis ditawarkan di dalam institusi medis. Yang pertama harus mematuhi Undang-Undang Farmasi dan Alat Kesehatan (PMD Act) dan mematuhi peraturan Good Gene, Cellular, and Tissue-based Products Manufacturing Practice (GCTP), yang mewajibkan fasilitas manufaktur yang sesuai dan kontrol manufaktur dan kualitas yang ketat. Di sisi lain, yang terakhir tunduk pada Undang-Undang tentang Menjamin Keamanan Pengobatan Regeneratif, yang mengharuskan penelitian klinis atau praktik medis swasta dilakukan.
Dukungan CM Plus terhadap Produk Pengobatan Regeneratif
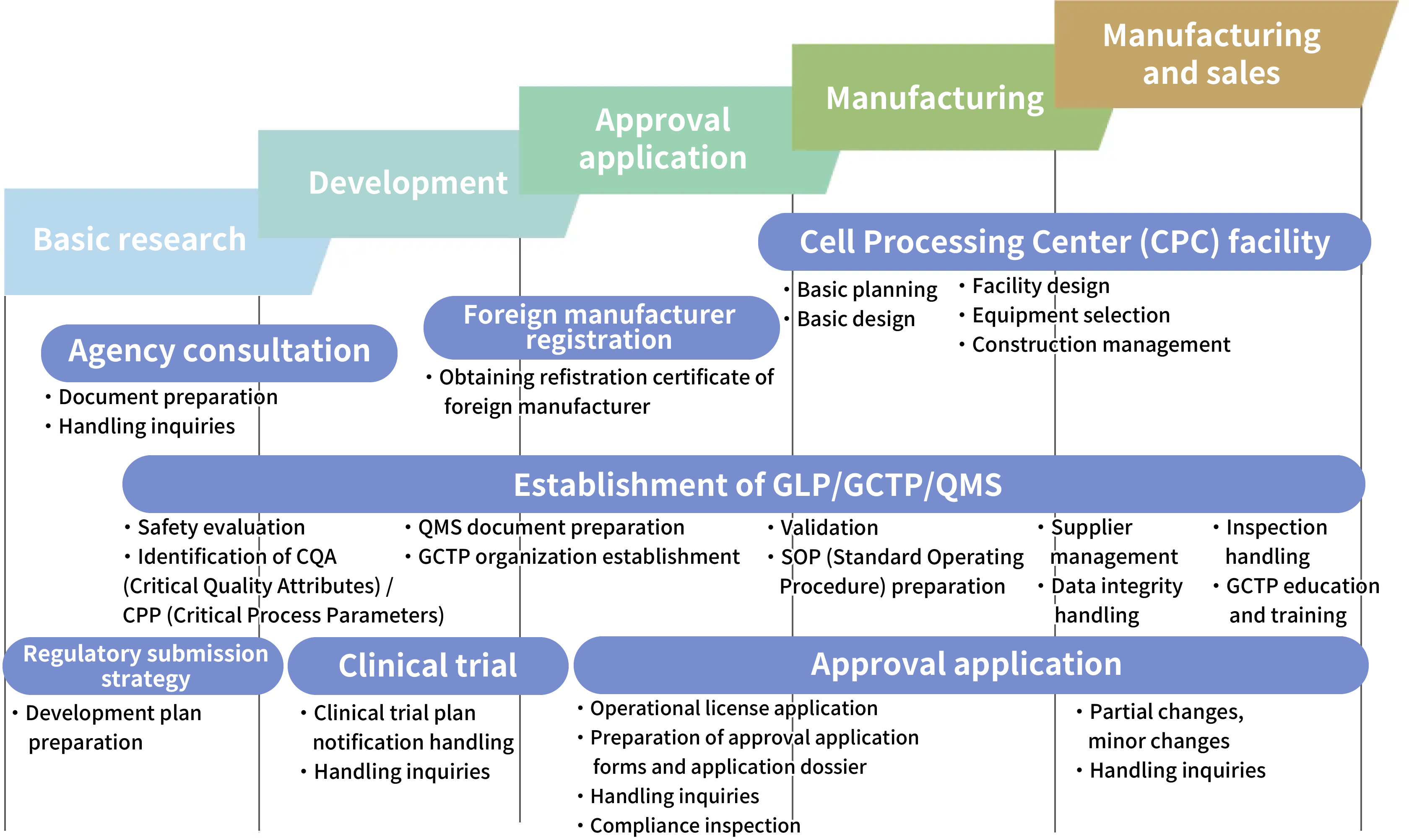
Langkah-langkah dari Pengembangan hingga Pembuatan dan Penjualan produk pengobatan regeneratif, dll.
CM Plus mendukung klien kami melalui setiap fase, dari penelitian dasar hingga pasca-pemasaran produk pengobatan regeneratif, dll.
CM Plus dapat membantu Anda jika Anda ingin:
- mempertimbangkan untuk memasuki industri pengobatan regeneratif dari bidang yang berbeda.
- membangun organisasi yang mematuhi GCTP.
- meningkatkan peralatan dari skala laboratorium ke skala komersial dan memerlukan dukungan untuk pemilihan peralatan dan keputusan spesifikasi.
- membuat dokumen yang mematuhi pendekatan berbasis risiko terkini.
- saran tentang apakah akan memiliki fasilitas CPC secara internal atau mengalihdayakannya
- melakukan validasi dan membuat SOP untuk produksi tetapi kekurangan sumber daya internal.
- melakukan analisis GAP untuk memeriksa apakah fasilitas Anda memenuhi persyaratan peraturan terbaru.
- seseorang yang akan mendampingi Anda untuk pra-konsultasi dan inspeksi dengan otoritas regulasi.
- menyewa lab dan memasang peralatan, dan perlu merencanakan tata letak yang mematuhi GCTP, dll.

Apa yang dapat dilakukan oleh Layanan Konsultasi Pengobatan Regeneratif CM Plus
- CM Plus memiliki konsultan di berbagai bidang. Di bidang pengobatan regeneratif, kami dapat menyediakan solusi terpadu untuk kebutuhan Anda dengan mengintegrasikan layanan konsultasi dan teknik. Baik itu strategi pengajuan regulasi dalam fase penelitian dan pengembangan, struktur organisasi GCTP, atau perencanaan fasilitas CPC dalam fase manufaktur, kami memiliki keahlian untuk mendukung Anda.
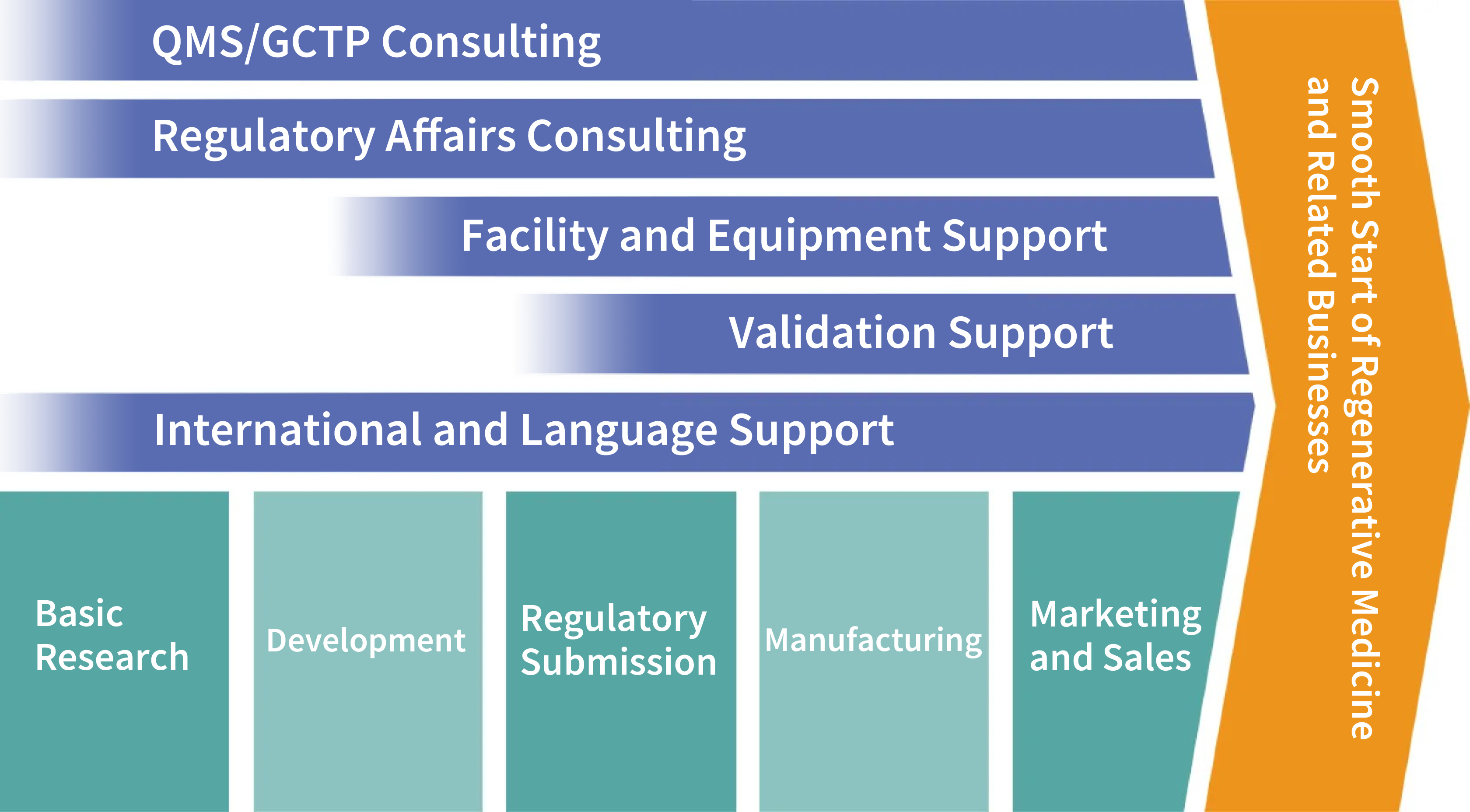
Layanan Satu Atap untuk Pengobatan Regeneratif oleh CM Plus
Konsultan dan teknisi pengobatan regeneratif kami yang sangat berpengalaman menyediakan layanan yang disesuaikan dengan kebutuhan spesifik Anda.

Konsultasi QMS/GCTP
-Dukungan untuk membangun organisasi yang mematuhi QMS dan GCTP
-Dukungan pendidikan GCTP
-Dukungan manajemen pemasok
-Dukungan analisis dan inspeksi GAP

Konsultasi Urusan Regulasi
-Dukungan untuk membuat rencana pengembangan
-Dukungan untuk berbagai konsultasi dengan Badan Farmasi dan Alat Kesehatan (BPOM)
-Dukungan untuk memperoleh izin produksi dan pemasaran/lisensi produsen/sertifikasi produsen asing (termasuk menanggapi pertanyaan)
-Persiapan aplikasi persetujuan dan dokumen terkait

Dukungan Konstruksi/ Diagnosis Fasilitas dan Peralatan
-Dukungan desain fasilitas, termasuk rencana dasar dan desain dasar untuk rencana konstruksi fasilitas GPC
-Dukungan untuk pemilihan peralatan dan pembuatan spesifikasi saat memperkenalkan peralatan produksi
-Manajemen konstruksi selama konstruksi fasilitas CPC

Dukungan Validasi
-Dukungan untuk membuat dokumentasi validasi saat memperkenalkan peralatan
-Pembuatan berbagai SOP
-Tugas Manajemen Validasi

Dukungan Bahasa Asing
-Dukungan untuk proyek pembangunan pabrik lintas batas
-Dukungan untuk memperoleh sertifikasi produsen asing
-Pengiriman penerjemah untuk inspeksi lintas batas
-Dukungan untuk persiapan dokumentasi bahasa Inggris
Contoh Penyelesaian Masalah Anda ①
(Untuk Perusahaan Pengobatan Regeneratif)

Kami sedang memulai bisnis pengobatan regeneratif. Kami memiliki jadwal yang padat, tetapi kami tidak tahu harus mulai dari mana dalam hal memperoleh izin pemasaran, lisensi produksi dan pemasaran, konfirmasi kepatuhan GCTP, dan pembangunan struktur organisasi.
Bagi klien dengan permasalahan seperti itu, CM Plus dapat memberikan dukungan sebagai berikut:


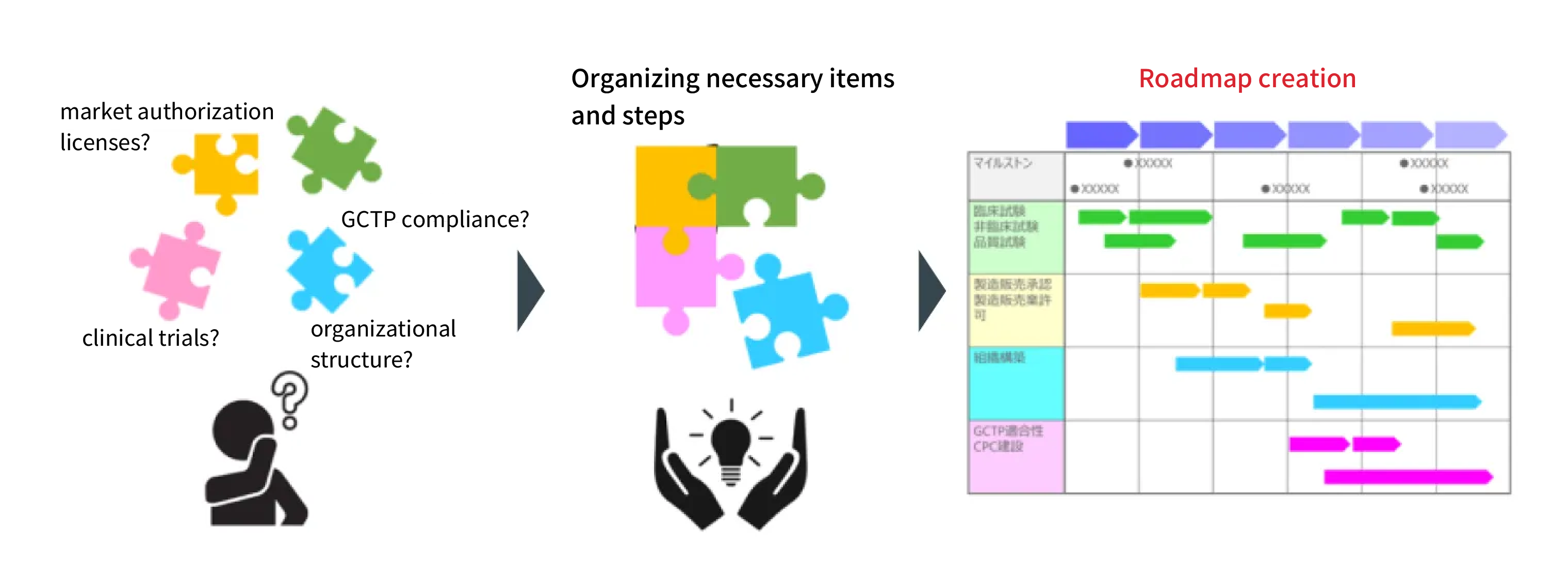
Menyusun Peta Jalan untuk Rencana Bisnis dan Pengembangan Pengobatan Regeneratif
Saat meluncurkan bisnis pengobatan regeneratif, penting untuk memiliki peta jalan (jadwal induk) yang dirancang dengan baik yang secara komprehensif mencakup semua prosedur dan investigasi yang diperlukan dalam urutan yang direncanakan dengan saksama. Pembuatan peta jalan ini memerlukan keahlian dan pengalaman tingkat tinggi, sehingga keterlibatan para ahli dengan pengetahuan tentang urusan regulasi, QMS, dan pengalaman pengembangan dalam bidang farmasi dan pengobatan regeneratif menjadi penting. CM Plus memiliki banyak konsultan yang mengkhususkan diri dalam bidang pengobatan regeneratif, pengajuan regulasi, dan konstruksi QMS. Kami dapat mendukung Anda dalam mengatur setiap langkah—mulai dari penelitian dasar, uji non-klinis, uji klinis, uji mutu, otorisasi pemasaran, lisensi manufaktur dan pemasaran, kepatuhan GCTP, dan sertifikasi produsen asing—dan dalam menyusun dan merencanakan peta jalan Anda.

Contoh Penyelesaian Masalah Anda ②
(Untuk Produsen Alat dan Produsen Reagen yang Mempertimbangkan Memasuki Industri Pengobatan Regeneratif)

Kami ingin mempromosikan produk Anda ke perusahaan pengobatan regeneratif, tetapi kami kurang memiliki pengetahuan tentang GCTP dan tidak yakin dalam menanggapi audit pemasok dari perusahaan pengobatan regeneratif.


Pendidikan GCTP, Pembentukan Struktur Organisasi, dan Audit Pemasok Tiruan
Di bidang pengobatan regeneratif, penting untuk mematuhi peraturan GCTP. CM Plus dapat memberikan dukungan edukasi GCTP dan konsultasi struktur organisasi yang sesuai dengan peraturan GCTP kepada produsen perangkat dan produsen reagen yang terlibat dalam industri pengobatan regeneratif. Kami juga menawarkan layanan seperti melakukan audit pemasok tiruan berdasarkan audit oleh perusahaan pengobatan regeneratif, melakukan pemeriksaan kepatuhan GCTP, dan melakukan analisis GAP. Kami menyediakan layanan terpadu yang unik dari CM Plus, yang menawarkan konsultasi dari berbagai perspektif, termasuk karakteristik produk, GCTP, peralatan, dan banyak lagi.


Konten Terkait
Wawasan Ahli
Silakan lihat juga artikel di situs penyebaran informasi kami, “Platform GMP,” yang dioperasikan oleh perusahaan kami.

Seri “Pengobatan Regeneratif dalam Praktik Klinis”

Seri “Pemikiran tentang Jaminan Kualitas untuk Pengobatan Regeneratif dan Produk Terkait”
(Hanya dalam bahasa Jepang)
Seri “Cara Membuat Dokumen Manufaktur untuk Insinyur Muda dalam Pengobatan Regeneratif”
(Hanya dalam bahasa Jepang)
“Pameran Produk Pengobatan Regeneratif & Terapi Sel” Akan Diadakan
Platform informasi ilmu hayati kami “iVEXL” akan menyelenggarakan “Pameran Produk Pengobatan Regeneratif & Terapi Sel.” Silakan kunjungi dan kumpulkan informasi.

Bertujuan untuk penerapan praktis pengobatan regeneratif dan produk terapi sel, kami akan menyatukan teknologi dan layanan terkini dari berbagai perusahaan, termasuk layanan kontrak seperti kultur sel, perangkat dan peralatan, serta solusi penyimpanan dan transportasi.
(Hanya dalam bahasa Jepang)