Dukungan bagi Pendatang Baru di Industri Alat Kesehatan
Pasar global untuk alat kesehatan diperkirakan mencapai sekitar 30 triliun yen, dengan sekitar 2,8 triliun yen di Jepang saja.
Pasar ini besar dan menarik bagi pendatang baru; namun, alat kesehatan tunduk pada peraturan ketat berdasarkan Undang-Undang tentang Menjamin Kualitas, Khasiat, dan Keamanan Produk Termasuk Farmasi dan Alat Kesehatan” (disingkat Undang-Undang Farmasi dan Perangkat Medis atau Undang-Undang PMD). Bahkan jika suatu bahan atau teknologi dapat diterapkan pada pengobatan, ada rintangan signifikan yang harus diatasi untuk memperkenalkannya sebagai alat kesehatan ke pasar.
CM Plus mendukung pendatang baru dengan membangun sistem manajemen mutu (QMS) berdasarkan Ordonansi QMS (ISO 13485) dan melakukan desain dan pengembangan produk sesuai dengan QMS sejak tahap perencanaan awal alat kesehatan, memastikan masuknya pasar dengan lancar dan tidak dapat diubah.”
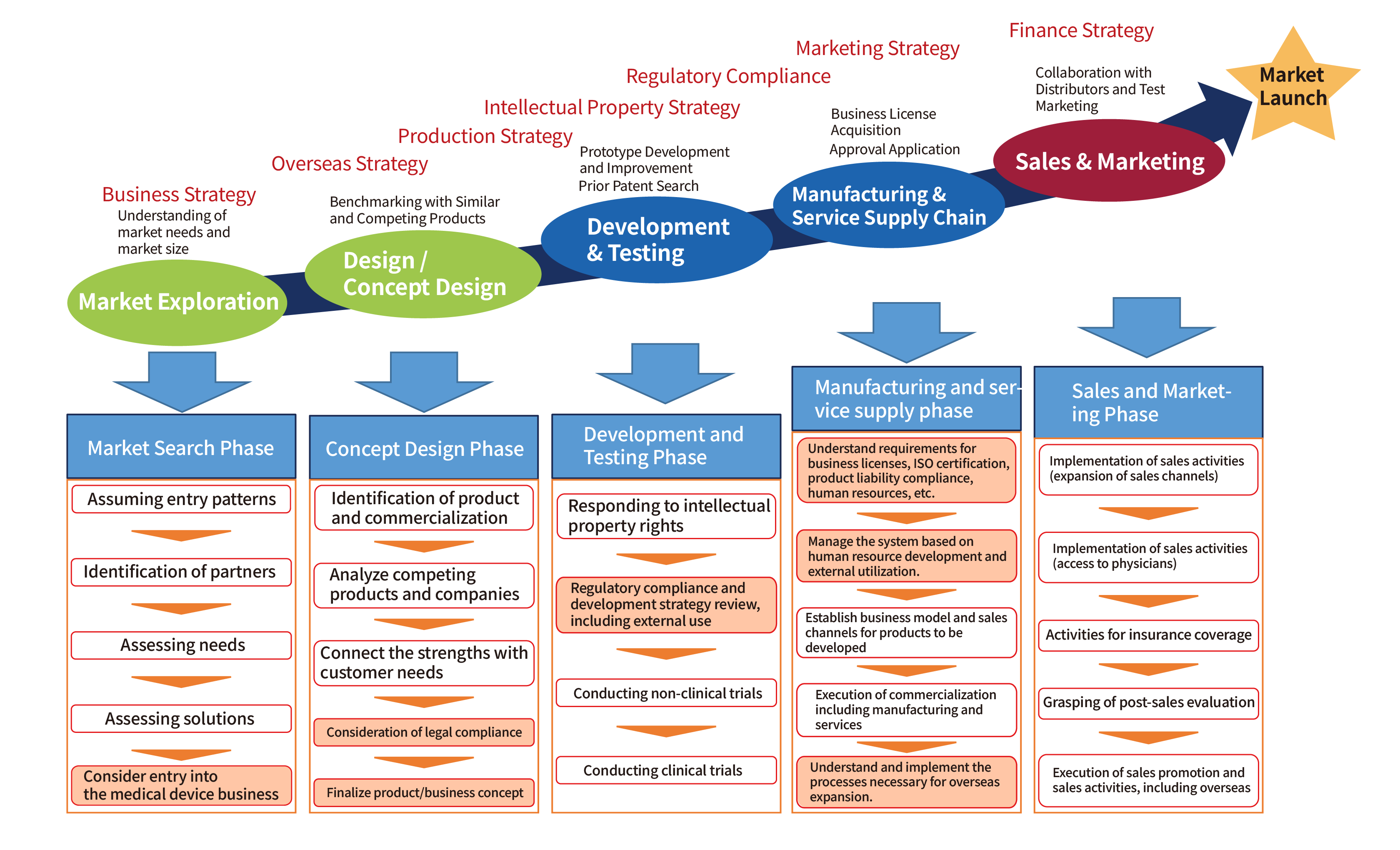
Peta Jalan dari Pengembangan hingga Peluncuran Pasar Alat Kesehatan
“Buku Pegangan Dukungan Pengembangan Alat Kesehatan” Direvisi pada Oktober 2023
Dari Sekretariat Kabinet (Kantor Strategi Kesehatan dan Medis), Kementerian Pendidikan, Kebudayaan, Olahraga, Sains dan Teknologi, Kementerian Kesehatan, Tenaga Kerja dan Kesejahteraan, dan Kementerian Ekonomi, Perdagangan dan Industri
※menunjukkan cakupan layanan konsultasi alat kesehatan CM Plus.
Contoh Langkah-Langkah Perkembangan di Jepang
 Perolehan Izin Pemasaran Alat Kesehatan dan Pendaftaran Usaha Manufaktur
Perolehan Izin Pemasaran Alat Kesehatan dan Pendaftaran Usaha Manufaktur
Pembuatan dan pemasaran alat kesehatan di Jepang harus mematuhi Undang-Undang Farmasi dan Alat Kesehatan (PMD Act). Untuk melakukan pembuatan dan pemasaran, diperlukan lisensi pemasaran alat kesehatan, dan untuk melakukan pembuatan, diperlukan pendaftaran sebagai badan usaha manufaktur.
 Penyusunan QMS (Quality Management System)
Penyusunan QMS (Quality Management System)
Untuk menjalankan serangkaian proses perancangan, pengembangan, produksi, pengiriman, dan penjualan peralatan medis, diperlukan Sistem Manajemen Mutu (SMM), dan pertama-tama, SMM harus ditetapkan. Di Jepang, hal ini ditetapkan oleh Peraturan Kementerian Kesehatan, Tenaga Kerja, dan Kesejahteraan No. 169 (Peraturan SMM). Peraturan No. 169 ini sebagian besar selaras dengan ISO 13485 (edisi 2016).
 Pemberitahuan, Aplikasi Sertifikasi, dan Aplikasi Persetujuan untuk Alat Kesehatan
Pemberitahuan, Aplikasi Sertifikasi, dan Aplikasi Persetujuan untuk Alat Kesehatan
Setelah rencana desain, pengembangan, dan manufaktur disiapkan untuk realisasi produk, pemberitahuan, aplikasi sertifikasi, atau aplikasi persetujuan untuk alat kesehatan diperlukan. Pilihan di antara ini bergantung pada tingkat risiko yang terkait dengan alat kesehatan.
Misalnya, jarum suntik tanpa jarum dikategorikan sebagai Kelas I dan memerlukan pemberitahuan, sedangkan jarum suntik dengan jarum termasuk Kelas II dan memerlukan aplikasi sertifikasi. Selain itu, perangkat seperti kateter yang dimasukkan ke dalam pembuluh darah memerlukan aplikasi persetujuan.
 Penilaian Kesesuaian QMS
Penilaian Kesesuaian QMS
Dalam hal permohonan sertifikasi atau permohonan persetujuan, penilaian kesesuaian QMS akan dilakukan setelah permohonan diajukan. Penilaian ini menentukan apakah praktik manajemen produksi dan manajemen mutu benar-benar diterapkan sesuai dengan Ordonansi QMS dan ISO 13485 (edisi 2016). Untuk sertifikasi, penilaian ini dilakukan oleh Badan Sertifikasi Terdaftar, dan untuk produk yang disetujui, penilaian ini dilakukan oleh PMDA (Badan Farmasi dan Alat Kesehatan).
 Lisensi Pemasaran
Lisensi Pemasaran
Dalam hal permohonan sertifikasi dan persetujuan, manufaktur dan pemasaran hanya mungkin dilakukan setelah permohonan lulus dan penilaian kesesuaian QMS telah berhasil diselesaikan.
Layanan Dukungan Masuk Pasar Baru oleh CM Plus
Seperti yang ditunjukkan pada contoh di atas, berbagai tugas muncul berdasarkan persyaratan regulasi selama tahap memasuki pasar baru. CM Plus mendukung pelaksanaan tugas-tugas ini. Kami menyediakan layanan yang sesuai dengan kebutuhan Anda, mulai dari dukungan proyek penuh hingga bantuan parsial, seperti validasi saja. Konten dukungan spesifiknya adalah sebagai berikut:
Penyusunan QMS
Kami membantu dalam penyusunan Sistem Manajemen Mutu (SMM) yang sepadat mungkin, yang disesuaikan dengan skala operasi Anda. Ini termasuk dukungan untuk persiapan dokumentasi yang diperlukan dan penerapan praktis sistem tersebut.

Dukungan untuk Kontrol Desain
Kami membantu dalam perancangan perangkat medis yang baru dikembangkan dengan membantu mengklarifikasi persyaratan, mengubahnya menjadi masukan, memajukan pekerjaan perancangan dan pengembangan aktual, membuat keluaran, memverifikasi keluaran, memvalidasi keluaran, dan melakukan tugas manajemen risiko pada titik-titik utama.

Dukungan untuk Persiapan Penilaian Kesesuaian QMS
Kami menyediakan bantuan dengan pekerjaan persiapan dan layanan seperti inspeksi tiruan untuk mengantisipasi inspeksi oleh badan sertifikasi dan PMDA.

Dukungan Validasi
Saat menyiapkan proses manufaktur di lokasi produksi, kami menyediakan dukungan yang komprehensif, mulai dari perencanaan validasi hingga peringkasan laporan.

Sistem Manajemen Mutu: Peningkatan Berkelanjutan Sistem Manajemen Mutu (QMS)
Alat Kesehatan merupakan alat untuk perawatan dan diagnosis, yang membutuhkan peningkatan kinerja berkelanjutan, peningkatan keselamatan, dan peningkatan berkelanjutan pada Sistem Manajemen Mutu (SMM) itu sendiri. Untuk mendukung peningkatan berkelanjutan ini, CM Plus menawarkan layanan berikut.
Selain itu, banyak produsen alat kesehatan tidak hanya menargetkan pasar domestik tetapi juga mengekspor ke berbagai negara di seluruh dunia. Persyaratan regulasi tidak hanya mencakup regulasi SMM Jepang tetapi juga standar internasional seperti ISO 13485 dan Regulasi Sistem Mutu (QSR) FDA AS. Ekspor memerlukan kepatuhan terhadap regulasi negara tujuan.
Peningkatan Berkelanjutan Sistem Manajemen Mutu
Optimalisasi Sistem Manajemen Mutu (QMS)
Kami sering melihat kasus di mana Sistem Manajemen Mutu itu sendiri menjadi membengkak dan sulit dikelola, berubah menjadi tumpukan dokumen karena koreksi berulang atas masalah yang ditunjukkan dalam audit berkala ISO 13485 sebelumnya. Kami mendukung rekonstruksi Sistem Manajemen Mutu yang ringkas dan mudah dioperasikan berdasarkan siklus PDCA, yang disesuaikan dengan skala fasilitas produksi dan jumlah barang yang diproduksi atau dijual.
Dukungan untuk Membangun Sistem Tinjauan Manajemen
Inti dari QMS adalah tinjauan manajemen yang melibatkan manajemen puncak secara langsung. CM Plus membantu mengoptimalkan konten tinjauan manajemen dan formatnya agar memudahkan manajemen puncak dalam mengambil keputusan.
Dukungan untuk Meninjau Sistem Tindakan Korektif dan Pencegahan
Masalah yang paling sering muncul dalam audit QMS eksternal terkait dengan tindakan korektif dan preventif. Apa tindakan korektif yang sebenarnya? Apa metode yang efektif untuk tindakan preventif? Dari perspektif ini, kami mengusulkan peninjauan ulang terhadap sistem saat ini.
Dukungan Kontrol Desain
Saat merancang perangkat medis baru, CM Plus mendukung hal-hal berikut:
- Klarifikasi persyaratan
- Konversi ke input
- Perkembangan pekerjaan desain dan pengembangan aktual
- Pembuatan output
- Verifikasi output
- Validasi output
- Manajemen risiko pada titik kritis
Selain itu, CM Plus menyediakan dukungan komprehensif untuk dokumentasi, mulai dari pembuatan protokol berdasarkan siklus PDCA hingga persiapan laporan.
Dukungan CSV (Validasi Sistem Terkomputerisasi)
Mengingat integrasi perangkat lunak ke dalam alat kesehatan, penjualan perangkat lunak mandiri, dan penggunaan perangkat lunak khusus dalam Sistem Manajemen Mutu, CSV (Validasi Sistem Terkomputerisasi) kini menjadi sangat penting. Kami membantu seluruh proses, mulai dari perencanaan CSV hingga pembuatan laporan.
Dukungan untuk Mempersiapkan Audit Kesesuaian QMS
Kami menawarkan layanan untuk membantu dalam persiapan awal untuk audit kesesuaian QMS oleh badan sertifikasi dan PMDA, termasuk audit tiruan.
Dukungan Validasi
Saat membangun proses produksi di fasilitas produksi, kami menyediakan dukungan komprehensif untuk validasi, mulai dari perencanaan hingga penyusunan laporan. Layanan kami khususnya mencakup validasi utilitas terkait untuk proses sterilisasi.
Untuk validasi fasilitas manufaktur dan peralatan bangunan, silakan lihat di sini.
CM Plus juga menawarkan konsultasi farmasi dan mampu menangani produk kombinasi (farmasi + alat kesehatan).
Konsultasi GMP/GDP Farmasi
Peningkatan GMP/GDP, dukungan inspeksi, pelatihan GMP/GDP, dukungan manajemen pemasok/manajemen pengadaan, dan layanan dukungan M&A lainnya.
Perkenalan untuk Layanan e-Learning
“Kursus Praktikum QMS Alat Kesehatan ISO 13485:2016”
Kami menyediakan pelatihan berbasis web untuk ISO 13485.
Poin-poin Penting dari Kursus Praktik QMS Alat Medis
Kursus ini menanggapi revisi ISO 13485 tahun 2016, yang mencakup hal-hal penting yang dipersyaratkan oleh ISO 13485 sekaligus menjelaskan “perubahan dalam peraturan yang direvisi pada tahun 2016” dan “implementasi praktis tertentu.”
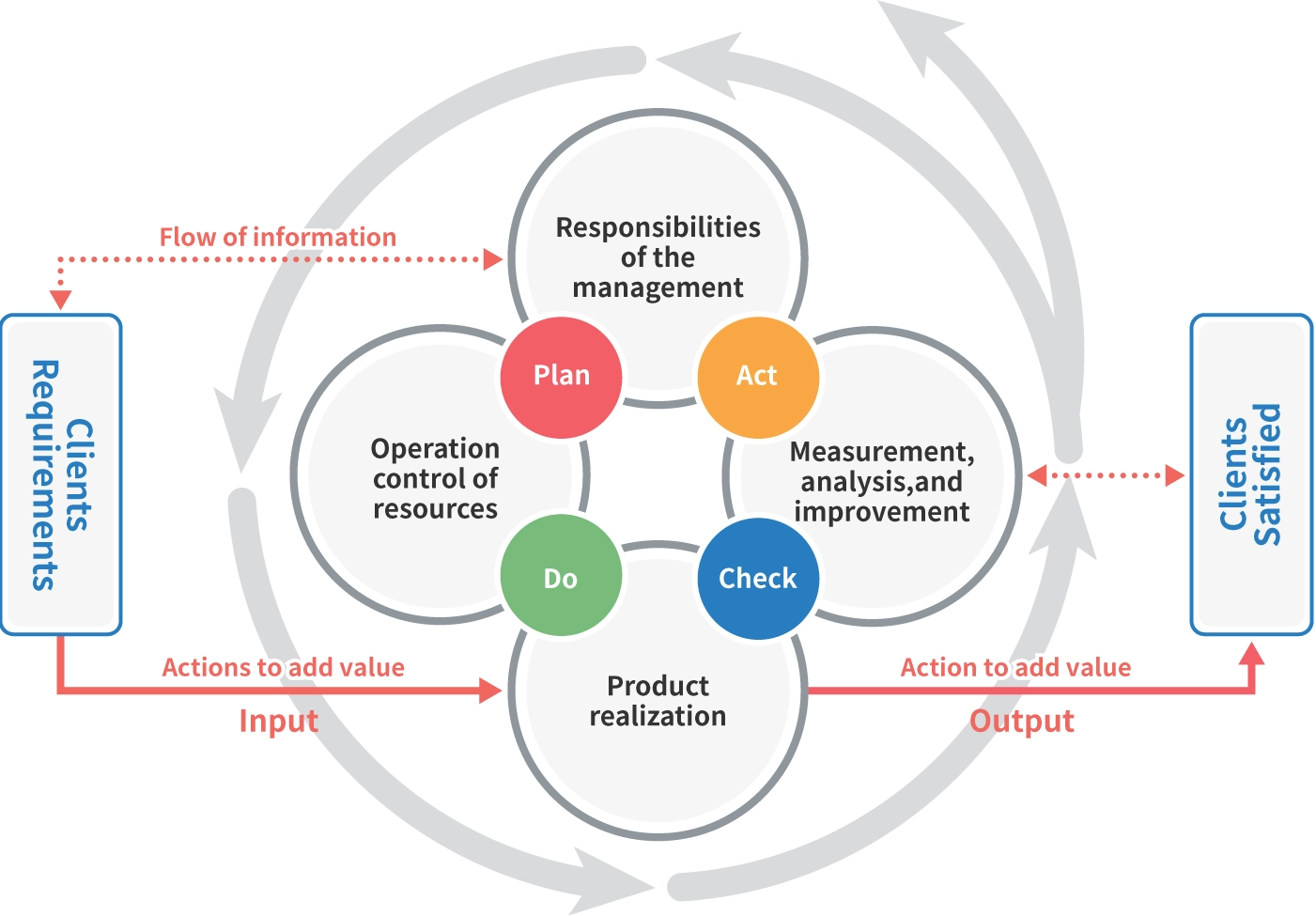
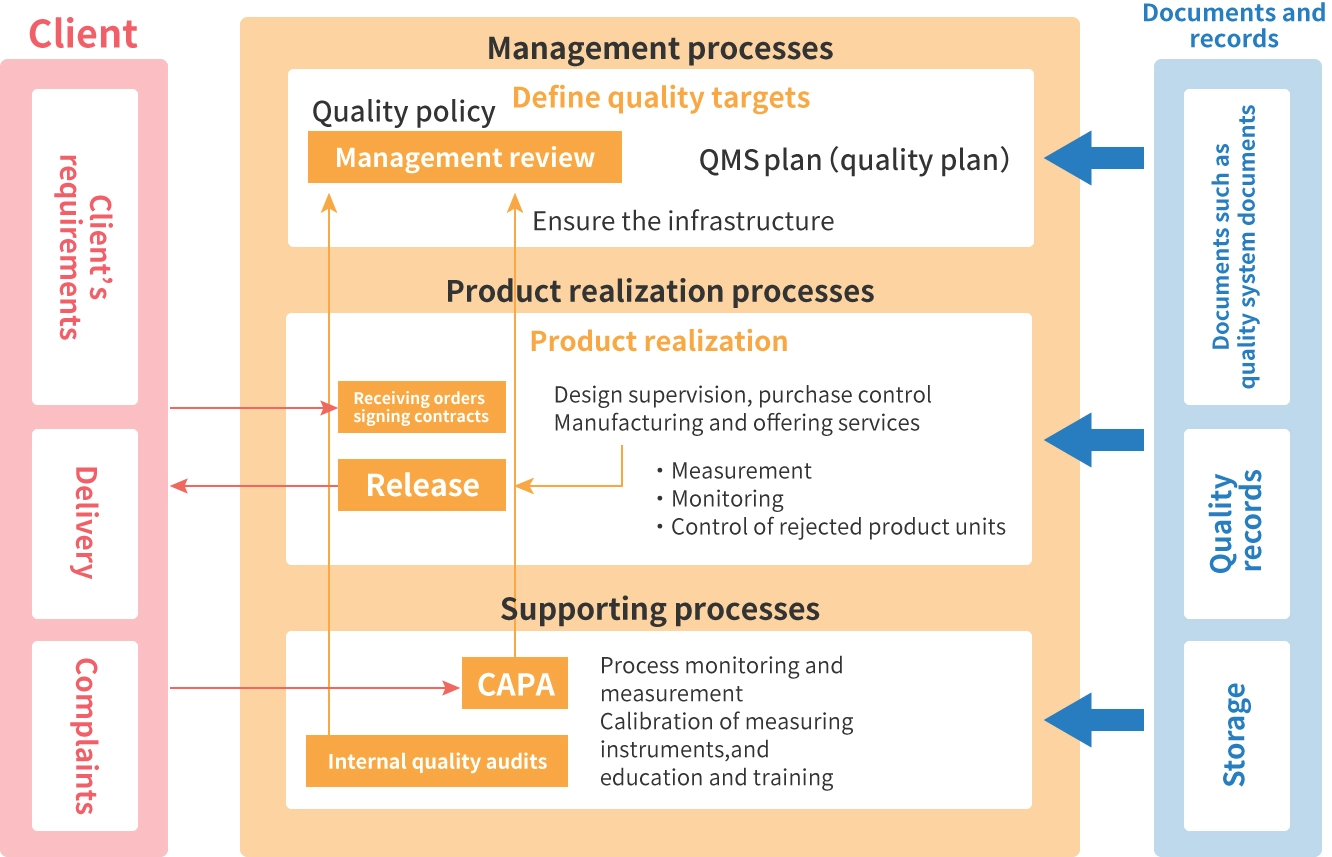
“Komentar tentang Diagram Proses Sistem Manajemen Mutu”
(Dari e-Learning kami, “Kursus Pelatihan Berorientasi Praktis tentang QMS untuk Perangkat Medis ISO 13485: Versi 2016.” Kursus 2 Sistem Manajemen Mutu)